��Ŀ����
����Ŀ������������Ҫ�Ļ��������ѧ��ѧ������������������������������⣬���������Ρ�FeSO4��7H2O��һ��dz��ɫ���壬�׳��̷��������ڴ����������������ӵķ�ˮ�������̷���ij������ˮ(����ǿ����������Cr2O![]() )���д�����
)�������
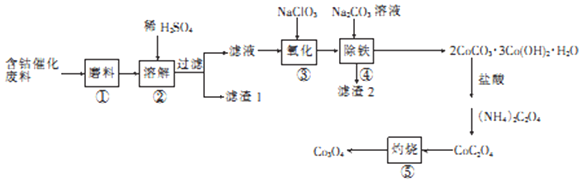
(1)�̷��������������ᷴӦ�����⣬��ҵ�ϻ����ÿ�����ˮ��������(��Ҫ�ɷ�ΪFeS2)����ȡ����֪�÷�Ӧ����������������������һ����ѧ��ѧ������ǿ�ᣬ��д���÷�Ӧ�Ļ�ѧ����ʽ��
________________________________________________________________________��
(2)����ƽ��________Fe2����________Cr2O![]() ��________===________Fe3����________Cr3����________H2O
��________===________Fe3����________Cr3����________H2O
(3)���÷�ˮ��������Cr3���ĺ���Ϊ1��10��2 mol��m��3��������83.4 kg�̷����Դ����÷�ˮ________��(��֪��ˮ���ܶ�Ϊ1 g��cm��3)��
���𰸡� 2FeS2��7O2��2H2O===2FeSO4��2H2SO4 6 1 14 H�� 6 2 7 1��104
����������1����������Ҫ�ɷ�ΪFeS2������ȡ����֪�÷�Ӧ����������������������һ����ѧ��ѧ������ǿ�ᣬ����ǿ������Ԫ���й�ֻ�������ᣬ����-1�۱��+6�ۣ�˵�����������ʿ����е�����������������Ӧ����ʽΪ2FeS2��7O2��2H2O===2FeSO4��2H2SO4 ��
��2��Fe2+��+2��+3������1����Cr2O72-��+6��+3������3��2��������С������Ϊ6��Ȼ����ݵ���غ㣬�������������������⣬��Ӧ���������Ӳ��뷴Ӧ��6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O��
��3���� ��2����֪ 6FeSO4��7H2O��2 Cr3+
6��278g 2mol
83400g n��Cr3+ ��
�� n��Cr3+ ��=100mol
���Է�ˮ�����Ϊ=107cm3�����Է�ˮ��Ϊ![]() 100mol=1��1010cm3 ��1��1010cm3 ��1g/cm3��
100mol=1��1010cm3 ��1��1010cm3 ��1g/cm3��![]() =1��104t��
=1��104t��