��Ŀ����
�Ƚ����ж����ԭ�ӵ�ԭ�ӹ���������ߵͣ�
��1��2s______3s����2��2s______3d��3��3d______4s��4��4f______6f��5��3px______3pz��
��1��2s______3s����2��2s______3d��3��3d______4s��4��4f______6f��5��3px______3pz��
��1����ͬ���Ӳ�����״��ͬ��ԭ�ӹ�������ĸߵ�˳��1s��2s��3s��4s��������2s��3s��
��2����ͬ�㲻ͬ�ܼ���ԭ�ӹ�������ĸߵ�˳��1s��2s��2p��3s��3p��4s��3d��4p��5s��4d��5p��6s��4f��������2s��3d
��3����ͬ�㲻ͬ�ܼ���ԭ�ӹ�������ĸߵ�˳��1s��2s��2p��3s��3p��4s��3d��4p��5s��4d��5p��6s��4f��������3d��4s��
��4����ͬ���Ӳ�����״��ͬ��ԭ�ӹ�������ĸߵ�˳��1s��2s��3s��4s��������4f��6f��
��5���ܲ㡢�ܼ�����ͬ��ԭ�ӹ��������ȣ�����3px=3pz��
�ʴ�Ϊ����1��������2��������3��������5��������6��=��
��2����ͬ�㲻ͬ�ܼ���ԭ�ӹ�������ĸߵ�˳��1s��2s��2p��3s��3p��4s��3d��4p��5s��4d��5p��6s��4f��������2s��3d
��3����ͬ�㲻ͬ�ܼ���ԭ�ӹ�������ĸߵ�˳��1s��2s��2p��3s��3p��4s��3d��4p��5s��4d��5p��6s��4f��������3d��4s��
��4����ͬ���Ӳ�����״��ͬ��ԭ�ӹ�������ĸߵ�˳��1s��2s��3s��4s��������4f��6f��
��5���ܲ㡢�ܼ�����ͬ��ԭ�ӹ��������ȣ�����3px=3pz��
�ʴ�Ϊ����1��������2��������3��������5��������6��=��

��ϰ��ϵ�д�
 Сѧ���AB��ϵ�д�
Сѧ���AB��ϵ�д� ABC����ȫ�ž�ϵ�д�
ABC����ȫ�ž�ϵ�д�
�����Ŀ
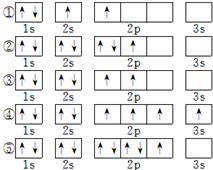
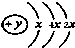 ����A��Bͬ���ڣ�B��C���γ����ӻ�����
����A��Bͬ���ڣ�B��C���γ����ӻ�����