题目内容
某学习小组为研究电化学原理,设计如图装置.下列叙述正确的是( )
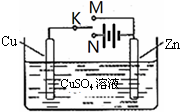

| A、K与M、N均断开时,该装置中无反应发生 |
| B、K与M、N均断开时,Zn表面有Cu析出 |
| C、K与M相连时,Cu2+往Zn极移动 |
| D、K与N相连时,Zn溶解,Cu片质量增加 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:锌比铜或活泼,K与M、N均断开时,锌可与硫酸铜溶液发生置换反应,K与M相连时,为铜锌原电池反应,锌为负极,铜为正极,K与N相连时,铜为阳极,锌为阴极,以此解答.
解答:
解:A、B.K与M、N均断开,发生的是化学腐蚀,锌和氯化铜反应生成铜,Zn+Cu2+=Cu+Zn2+,Zn表面有Cu析出,故A错误、B正确;
C.K与M相连时,为铜锌原电池反应,锌为负极,铜为正极,阳离子向正极移动,故C错误;
D.与N相连时,铜为阳极,锌为阴极,则铜片质量减小,锌片质量增加,为电镀铜的装置,故D错误.
故选B.
C.K与M相连时,为铜锌原电池反应,锌为负极,铜为正极,阳离子向正极移动,故C错误;
D.与N相连时,铜为阳极,锌为阴极,则铜片质量减小,锌片质量增加,为电镀铜的装置,故D错误.
故选B.
点评:本题综合考查了原电池和电解质知识,为高频考点,侧重于电解池原理的分析判断,电极判断和电极反应等知识,注意把握原电池和电解池的工作原理,难度不大.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
如图是一些常见有机物的转化关系,以下有关反应的说法不正确的是( )
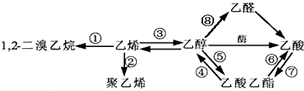

| A、反应①是加成反应 |
| B、反应②是加聚反应 |
| C、反应③是消去反应 |
| D、反应④⑤⑥是取代反应 |
下列依据相关实验得出的结论正确的是( )
| A、向某溶液中滴加盐酸,无现象,再加氯化钡溶液有白色沉淀,则该溶液中一定含SO42- |
| B、若向氯水中加入少量CaCO3固体,会使溶液的pH减小,HClO浓度增大 |
| C、将某气体通入溴水中,溴水颜色褪去,该气体一定是二氧化硫 |
| D、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
在实验室中,下列除去杂质的方法正确的是( )
| A、溴苯中混有溴,加入KI溶液,振荡,再用汽油萃取 |
| B、硝基苯中混有浓硝酸和浓硫酸,将其倒入到NaOH溶液中,静置,分液 |
| C、乙烷中混有乙烯,通氢气在一定条件下反应,使乙烯转化为乙烷 |
| D、乙烯中混有SO2和CO2,将其先后通入NaOH和KMnO4溶液中洗气 |
下列有关说法正确的是( )
| A、反应NH3(g)+HCl(g)═NH4Cl(s)在室温下可自发进行,则该反应的△H<0 |
| B、Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
| C、向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 |
| D、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
下列说法不正确的是( )
| A、芳香烃主要来源于分馏煤焦油和石油的催化重整 |
| B、苯的同系物均可被酸性高锰酸钾溶液氧化 |
| C、含苯环的烃都是芳香烃 |
| D、用分子筛固体催化剂工艺生产乙苯,可大幅度降低对环境的污染,提高环境效益 |
下列各组离子,在pH=0的溶液中可以大量共存的是( )
| A、Al3+、S2-、Br-、SO32- |
| B、Mg2+、Cu2+、SO42-、Br- |
| C、Na+、Fe2+、I-、MnO4- |
| D、NH4+、K+、HS-、Cl- |
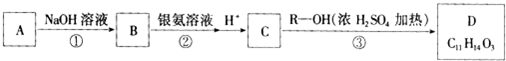 C在一定条件下可发生反应,生成一种高分子化合物E,E的结构简式为
C在一定条件下可发生反应,生成一种高分子化合物E,E的结构简式为 ,其中R、R′为烃基.请回答以下问题:
,其中R、R′为烃基.请回答以下问题: ,且属于酯的所有同分异构体的结构简式
,且属于酯的所有同分异构体的结构简式