题目内容
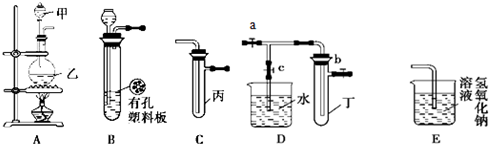
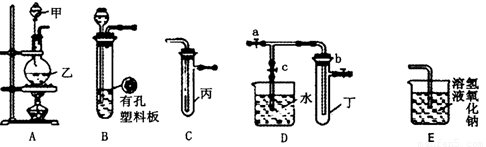
为验证Cl2、Br2的氧化性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如下图,填写图中的空白。

(1)2 mL 试剂 ;加入少量 试剂;再加入
试剂; 现象: 。
(2)可以证明Cl2的氧化性____________(填“强于”或“弱于”)Br2的氧化性;氯元素的非金属性 ____________(填“强于”或“弱于”)_溴元素的非金属性。
( 3 )此反应的离子方程式为:________________________________________。
(4)某溶液中Cl-、Br-、I-的物质的量之比为4∶1∶4,要使溶液中的Cl-、Br-、I-的物质的量之比变为7∶1∶1,则通入Cl2的物质的量与原溶液中I-的物质的量之比为______。
(1)NaBr溶液 ; 氯水 ; 四氯化碳 ; 分成两层 上层无色、下层棕红色(或橙色或橙红色) 。
(2)强于;强于(3)Cl2+2Br-=2Cl-+Br2
(4)3:8
【解析】
试题分析:(1)验证Cl2、Br2的氧化性强弱,结合题干提供的试剂,可知第一支试管应该装的是2mLNaBr溶液,第二支试管中加入氯水,振荡之后再加入CCl4把置换出来的Br2从混合液中萃取出来,混合液分成两层,上层为NaCl溶液无色,下层Br2和CCl4,呈棕红色(或橙色或橙红色)。
(2)由实验证明Cl2的氧化性强于Br2的氧化性,结合元素周期律,也可得氯元素的非金属性强于溴元素的非金属性。该反应的离子方程式为:Cl2+2Br-=2Cl-+Br2 。
(4)依题意,可设原溶液中Cl-、Br-、I-的物质的量为4X、X、4X,反应后溶液中的Cl-、Br-、I-的物质的量为7X、X、X,通入氯气后,发生如下反应:Cl2+2I-=2Cl-+I2,可知I-的减少量为Cl2通入量的2倍,则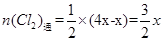 ,
,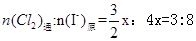 。
。
考点:化学实验,卤素的化学性质,物质的量计算。
点评:探究式实验是近年来高考的热点,重在培养学生的发散性思维,逻辑思维能力,本题难度不大,解题的关键是要掌握卤素的化学性质和反应方程式的正确书写,结合反应原理,题干信息,巧妙假设,化繁为简。

 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案