题目内容
(2011?四川二模)已知2X(g)+Y(g)?mZ(g);△H=-akJ/mol(a>0).现有甲、乙两容积相等且固定的密闭容器,保持温度不变的条件下,向甲容器中通入2mol X和1mol Y,达平衡状态时,放出热量为bkJ,向乙容器中通入1mol X和0.5mol Y,达平衡状态时,放出热量为ckJ,且b>2c.则a、b、m的关系可能正确的是( )
分析:A、根据热化学反应方程式中的反应热是物质完全转化的能量与化学平衡中不完全转化的关系来分析;
B、讨论m的情况,根据压强对平衡的影响可知,增大压强,化学平衡向气体体积缩小的方向移动的程度大,及b、c的关系来分析m的大小;
C、讨论m的情况,根据压强对平衡的影响可知,增大压强,化学平衡向气体体积缩小的方向移动的程度大,及b、c的关系来分析m的大小;
D、根据热化学反应方程式中的反应热是物质完全转化的能量与化学平衡中不完全转化的关系来分析.
B、讨论m的情况,根据压强对平衡的影响可知,增大压强,化学平衡向气体体积缩小的方向移动的程度大,及b、c的关系来分析m的大小;
C、讨论m的情况,根据压强对平衡的影响可知,增大压强,化学平衡向气体体积缩小的方向移动的程度大,及b、c的关系来分析m的大小;
D、根据热化学反应方程式中的反应热是物质完全转化的能量与化学平衡中不完全转化的关系来分析.
解答:解:A、因该反应为可逆反应,a为2molX、1molY反应完全转化时放出的能量,而向密闭容器甲中通入2molX和1molY,不会完全转化,则a>b,故A错误;
B、因为定容,若m<3,乙中压强比甲中压强小,平衡向体积增大方向移动趋势大,逆向移动的趋势大,乙中物质的转化率较小,放出的热量b>2c,与题中热量关系符合,故B正确;
C、因为定容,若m>3,乙中压强比甲中压强小,平衡向体积增大方向移动趋势大,平衡正向移动,乙中物质转化率较大,放出的热量b<2c,与题目中b>2c不符,故C错误;
D、因该反应为可逆反应,a为2molX、1molY反应完全转化时放出的能量,而向密闭容器甲中通入2molX和1molY,不会完全转化,则a>b,故D错误.
故选B.
B、因为定容,若m<3,乙中压强比甲中压强小,平衡向体积增大方向移动趋势大,逆向移动的趋势大,乙中物质的转化率较小,放出的热量b>2c,与题中热量关系符合,故B正确;
C、因为定容,若m>3,乙中压强比甲中压强小,平衡向体积增大方向移动趋势大,平衡正向移动,乙中物质转化率较大,放出的热量b<2c,与题目中b>2c不符,故C错误;
D、因该反应为可逆反应,a为2molX、1molY反应完全转化时放出的能量,而向密闭容器甲中通入2molX和1molY,不会完全转化,则a>b,故D错误.
故选B.
点评:本题考查热化学方程式、平衡移动,难度中等,明确热化学方程式的意义及根据热量判断物质的转化率大小是解答的关键.BC采取讨论方法,较麻烦但容易接受,可以根据热量直接判断转化率大小,在利用压强对平衡影响判断.

练习册系列答案
相关题目
 (其中R为饱和烃基),A在一定条件下有如图所示的转化关系.已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2.
(其中R为饱和烃基),A在一定条件下有如图所示的转化关系.已知E的蒸气密度是相同条件下H2密度的74倍,分子组成符合CaHbO2.





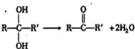 ,对于某有机物
,对于某有机物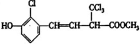 下列说法正确的是( )
下列说法正确的是( )