题目内容
2.用双线桥法标出电子转移情况:3BrF3+5H2O═HBrO3+Br2+O2+9HF,当180g水都做还原剂时,被自身还原的BrF3 是$\frac{10}{3}$ mol.分析 在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,元素化合价变化情况为:溴元素由+3价升高为+5价,溴元素由+3价降低为0价,氧元素化合价由-2价升高为0价,所以BrF3既起氧化剂也起还原剂作用,同时水也起还原剂作用.根据氧化还原反应中电子转移守恒计算自身还原的BrF3的物质的量.
解答 解:n(H2O)=$\frac{180g}{18g/mol}$=10mol,
在反应3BrF3+5H2O=HBrO3+Br2+9HF+O2中,元素化合价变化情况为:溴元素由+3价升高为+5价,溴元素由+3价降低为0价,氧元素化合价由-2价升高为0价,所以BrF3既起氧化剂也起还原剂作用,同时水也起还原剂作用.
电子转移的方向可数目为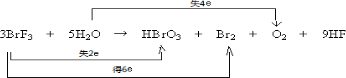 ,
,
由方程式可知5mol水参加反应有2mol水被氧化,3molBrF3参加反应,则10mol被氧化,则有15molBrF3参加反应,
其中5molBrF3为氧化剂,共得到15mol电子,10molBrF3为还原剂,失去电子数为10mol,
则自身还原的BrF3 是$\frac{10}{3}$mol,
故答案为: ;$\frac{10}{3}$.
;$\frac{10}{3}$.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应转移电子的考查,注意从元素的化合价角度分析,题目难度不大.

练习册系列答案
相关题目
13.有关热化学方程式书写与对应表述均正确的是( )
| A. | 稀硫酸与0.1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=+57.3 kJ•mol-1 | |
| B. | 在101KPa下氢气的燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| C. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热为110.5 kJ•mol-1 | |
| D. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 |
10.下列各组元素性质递变错误的是( )
| A. | P、S、Cl原子半径依次减小 | |
| B. | Li、Na、K、Rb的金属性依次增强 | |
| C. | N、O、F最高正价依次升高 | |
| D. | Li、Be、B原子最外层电子数逐渐增多 |
14.下列溶液中的Cl-的物质的量与50mL1mol•L-1 AlCl3溶液中Cl-的物质的量相等的是( )
| A. | 150mL1mol•L-1 氯化钠溶液 | B. | 75mL 1.5mol•L-1氯化钙溶液 | ||
| C. | 150mL3mol•L-1 氯化钾溶液 | D. | 75mL 1mol•L-1 氯化铁溶液 |