题目内容
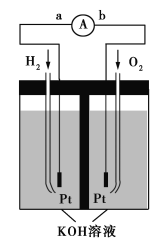
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。
请回答:
(1)氢氧燃料电池的能量转化主要形式是________________,在导线中电子流动方向为________________(用a、b表示)。
(2)负极反应式为_____________________________________。
(3)电极表面镀铂粉的原因为____________________________。
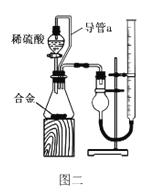
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2![]() 2LiH
2LiH
Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅰ中的还原剂是________,反应Ⅱ中的氧化剂是_____。
②已知LiH固体密度为0.82 g·cm-3,用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为_______________。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为_________mol。
【答案】(1)由化学能转变为电能 由a到b
(2)2H2+4OH--4e-===4H2O(或H2+2OH--2e-===2H2O)
(3)增大电极单位面积吸附H2、O2分子数,加快电极反应速率
(4)①Li H2O ②1∶1 148 ③32
【解析】(1)氢氧燃料电池中,负极通H2,正极通O2,所以导线中电子由a到b。
(2)负极H2被氧化,写电极反应式时要注意电解质溶液的组成。
(3)本题考查读题能力,铂粉作用在题设中有说明。
(4) ②2Li+H2![]() 2LiH
2LiH
22.4 L 16 g
吸收224 L H2时,生成的LiH的质量为160 g,LiH体积与被吸收的H2体积比为:![]() ∶224 L=1∶1 148。
∶224 L=1∶1 148。
③LiH+H2O === LiOH+H2↑
8 g 1 mol
160 g LiH与H2O作用生成20 mol H2,H2完全被氧化失40 mol电子,若能量转化率为80%,则导线中通过的电子的物质的量为40 mol×80%=32 mol。