题目内容
18.一定温度下,在一个固定容积的密闭容器里发生N2(g)+3H2(g)?2NH3(g)反应,此反应达到化学平衡状态的标志是:①N2,H2和NH3的浓度不再改变,②v正(NH3)=2v逆(N2),③c(N2):c(H2):c(NH3)=1:3:2,④单位时间里每增加1molN2,同时增加3molH2( )| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | 只有①② |
分析 反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断.
解答 解:①达到平衡时,正逆反应速率相等,即各种物质的消耗速率等于其生成速率,从而浓度不再发生变化,故①正确;
②化学反应达平衡的根本标志是v正=v逆,现在化学反应速率之比与化学计量数之比相等,且反应速率方向相反,故可以作为平衡的标志,故②正确;
③反应达平衡时,只是各物质的浓度不变而已,各物质的浓度之间无必然的数值关系,即c(N2):c(H2):c(NH3)=1:3:2时不一定平衡,故③错误;
④单位时间里每增加1molN2,必然同时增加3molH2,与反应是否达平衡无关,即不能说明反应达平衡,故④错误.
故选D.
点评 本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
8.下列反应属于吸热反应的是( )
| A. | 钠与水反应 | B. | 镁带在空气中燃烧 | ||
| C. | 碳酸钙高温分解 | D. | 硝酸与氢氧化钠反应 |
9.既能与盐酸反应,又能与NaOH溶液反应的是( )
①(NH4)2CO3 ②Al(OH)3 ③NaHCO3 ④Al2O3 ⑤Fe(NO3)2.
①(NH4)2CO3 ②Al(OH)3 ③NaHCO3 ④Al2O3 ⑤Fe(NO3)2.
| A. | ①②③④ | B. | ②③④ | C. | ②④⑤ | D. | 全部 |
6.以下物质间的每步转化通过一步反应就能实现的是( )
| A. | N2→NO2→HNO3 | B. | Fe→FeCl3→FeCl2 | ||
| C. | Si→H2SiO3→Na2SiO3 | D. | Al2O3→Al(OH)3→NaAlO2 |
13.下列溶液加热蒸干后,能析出溶质固体的是( )
| A. | AlCl3 | B. | NH4HCO3 | C. | KHCO3 | D. | Fe2 (SO4)3 |
7.下列说法正确的是( )
①向某溶液中加盐酸,有能使澄清石灰水变浑浊的气体生成,则原溶液中有CO${\;}_{3}^{2-}$
②向某溶液中加氯化钡溶液,生成白色沉淀,再加盐酸沉淀不溶解,则原溶液中SO${\;}_{4}^{2-}$
③向某溶液中加硝酸银溶液,生成白色沉淀,则原溶液中有Cl-.
①向某溶液中加盐酸,有能使澄清石灰水变浑浊的气体生成,则原溶液中有CO${\;}_{3}^{2-}$
②向某溶液中加氯化钡溶液,生成白色沉淀,再加盐酸沉淀不溶解,则原溶液中SO${\;}_{4}^{2-}$
③向某溶液中加硝酸银溶液,生成白色沉淀,则原溶液中有Cl-.
| A. | ①② | B. | ①③ | C. | ②③ | D. | 都不确定 |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 4.6g的乙醇中含有的共价键的数目为0.6NA | |
| B. | 标准状况下,22.4L CHCl3含有的原子数是5NA | |
| C. | 氢氧化燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75NA |
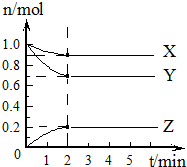 (1)某温度下,在一个2L密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如右图所示.
(1)某温度下,在一个2L密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如右图所示.
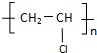 ;
; .
. .
.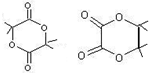 (写出一个即可).
(写出一个即可).