题目内容
【题目】将碱溶液A、盐溶液B按如下程序进行实验,根据下述现象判断: 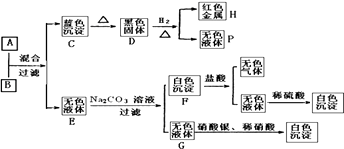
(1)A和B中溶质的化学式A;B、 .
(2)完成下列转化的化学方程式,是离子反应的只写离子方程式.
①A+B→C+E:;
②D+H2→H+P:;
③E+Na2CO3→F+G:;
④F+盐酸→I+E: .
【答案】
(1)Ba(OH)2;CuCl2
(2)Cu2++2OH﹣=Cu(OH)2↓;H2+CuO ![]() Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O
Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O
【解析】解:由转化关系图可知,红色金属H为Cu,蓝色沉淀C为Cu(OH)2 , 加热氢氧化铜时,氢氧化铜分解生成黑色固体D为CuO,氧化铜被氢气还原生成铜和水,所以P为H2O;碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,B为铜盐,由无色溶液E和碳酸钠溶液反应生成白色沉淀F及G,G的溶液中加入硝酸银、硝酸得到白色沉淀,故G为氯化钠,无色溶液E含有Cl﹣ , 故盐溶液B为CuCl2 , F为碳酸盐,F和盐酸反应生成无色气体和无色溶液,该无色溶液和稀硫酸反应生成白色沉淀,故无色溶液含有Ba2+ , 故白色沉淀F为BaCO3 , 无色溶液E含有Cl﹣ , 故E为BaCl2 , 再结合碱溶液A+盐溶液B→Cu(OH)2+无色溶液E,故A为Ba(OH)2 , 验证符合转化关系,(1)通过以上分析知,A溶液和B溶液的溶质分别是Ba(OH)2、CuCl2 , 所以答案是:Ba(OH)2、CuCl2;(2)①A+B→C+E是氢氧化钡与氯化铜反应生成氢氧化铜与氯化钡,反应离子方程式为:Cu2++2OH﹣=Cu(OH)2↓;②D+H2→H+P是氢气和氧化铜发生氧化还原反应生成铜和水,反应方程式为:H2+CuO ![]() Cu+H2O;③E+Na2CO3→F+G是氯化钡与碳酸钠反应生成碳酸钡与氯化钠,反应离子方程式为:Ba2++CO32﹣=BaCO3↓;④F+盐酸→I+E是碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,
Cu+H2O;③E+Na2CO3→F+G是氯化钡与碳酸钠反应生成碳酸钡与氯化钠,反应离子方程式为:Ba2++CO32﹣=BaCO3↓;④F+盐酸→I+E是碳酸钡与盐酸反应生成氯化钡、二氧化碳与水,反应离子方程式为:BaCO3+2H+=Ba2++CO2↑+H2O,
所以答案是:Cu2++2OH﹣=Cu(OH)2↓;H2+CuO ![]() Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O.
Cu+H2O;Ba2++CO32﹣=BaCO3↓;BaCO3+2H+=Ba2++CO2↑+H2O.

【题目】下列实验与对应示意图的关系正确的是( )
A | B | C | D |
NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
|
|
|
|
A.A
B.B
C.C
D.D