题目内容
(1)为了保护环境,变害为利,工业上常用纯碱吸收有害气体SO2,同时得到亚硫酸氢钠,该反应的离子方程式是__________。从这一反应可见H2SO3的酸性比H2CO3的酸性________________。亚硫酸钠常用于除去漂白织物后剩余的游离氯,该反应的离子方程式为________________。(2)近年来医学界发现,铝对人体健康危害性很大,能引起痴呆、骨痛、贫血、甲状腺功能降低、胃液分泌减少等多种疾病。为了防止铝对人体的慢性中毒,不要用铝锅来烹调酸、碱性强的食品,原因是____________。
解析:(1)H2SO3的酸性比H2CO3强,用Na2CO3吸收SO2,题目已指出产物是NaHSO3,不要误写为Na2SO3;题目已要求写离子方程式,不要写化学方程式。
Cl2具有强氧化性,可将![]() 氧化为
氧化为![]() ,为
,为![]() 提供氧原子的是水。
提供氧原子的是水。
(2)铝锅表面是一层致密的氧化物保护膜——Al2O3。Al和Al2O3都是既能与强酸反应,又能与强碱反应,这里主要是Al2O3与强酸或强碱的反应。
答案:(1)2SO2+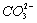 +H2O══2
+H2O══2![]() +CO2↑ 强
+CO2↑ 强 ![]() +Cl2+H2O══
+Cl2+H2O══![]() +2Cl-+2H+
+2Cl-+2H+
(2)铝和氧化铝都能跟酸、碱作用生成能被人体吸收的可溶性铝盐和偏铝酸盐:2Al+6H+══2Al3++3H2↑,2Al+2OH-+2H2O══2![]() +3H2↑,Al2O3+6H+══2Al3++3H2O,Al2O3+2OH-══2
+3H2↑,Al2O3+6H+══2Al3++3H2O,Al2O3+2OH-══2![]() +H2O。
+H2O。

练习册系列答案
相关题目