题目内容
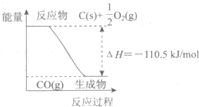 (2010?西城区一模)反应2C+O2=2CO的能量变化如图所示.下列说法正确的是( )
(2010?西城区一模)反应2C+O2=2CO的能量变化如图所示.下列说法正确的是( )分析:根据图示可知C(s)+
O2(g)=2CO(g)△H=-110.5kJ/mol.
A、反应生成14g CO(g)时,12g碳未全部反应;
B、一氧化碳反应生成二氧化碳过程是放热反应;
C、焓变单位为KJ/mol;
D、焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量.
| 1 |
| 2 |
A、反应生成14g CO(g)时,12g碳未全部反应;
B、一氧化碳反应生成二氧化碳过程是放热反应;
C、焓变单位为KJ/mol;
D、焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量.
解答:解:A、12 g C(s)与一定量O2(g)反应生成28 g CO(g)放出的热量为110.5 kJ,故A错误;
B、2mol C(s)与足量O2(g)反应生成CO2(g),反应过程中一氧化碳生成二氧化碳是放热反应,所以放出的热量大于221kJ,故B正确;
C、该反应的热化学方程式是2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,故C错误;
D、该反应的反应热等于O2分子和碳中化学键断裂时所吸收的总能量与CO分子中化学键形成时所释放的总能量的差,故D错误;
故选B.
B、2mol C(s)与足量O2(g)反应生成CO2(g),反应过程中一氧化碳生成二氧化碳是放热反应,所以放出的热量大于221kJ,故B正确;
C、该反应的热化学方程式是2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,故C错误;
D、该反应的反应热等于O2分子和碳中化学键断裂时所吸收的总能量与CO分子中化学键形成时所释放的总能量的差,故D错误;
故选B.
点评:本题考查反应能量变化分析,反应焓变理解和计算方法,图象分析判断能力,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
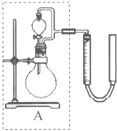 (2010?西城区一模)过氧化氢对环境友好,性质多样,有很重要的研究和应用价值.
(2010?西城区一模)过氧化氢对环境友好,性质多样,有很重要的研究和应用价值. (2010?西城区一模)甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系.甲+乙→丙+丁
(2010?西城区一模)甲、乙、丙、丁是由短周期元素组成的物质,它们之间存在如下转化关系.甲+乙→丙+丁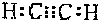
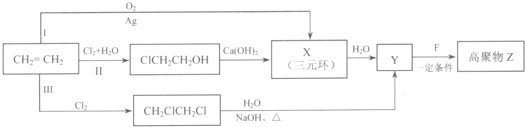
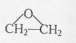
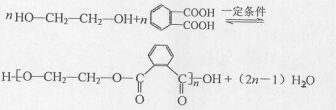
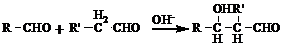 (R、R'代表烃基或氢原子)
(R、R'代表烃基或氢原子)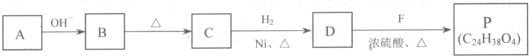
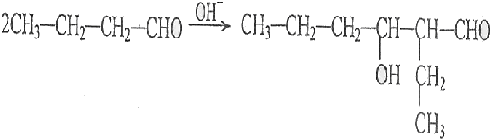
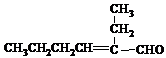
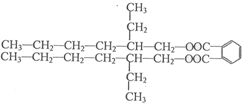
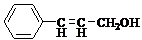 )的合成路线:
)的合成路线: