题目内容
【化学——选修3:物质结构与性质】某配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4︰4︰5︰1︰1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)d n+6nsl。回答下列问题。
(1)元素D在周期表中的位置是 ,B原子的外围电子排布图为 。E原子的核外有 种不同运动状态的电子,B和C的第一电离能大小关系是 。(用元素符号表示)
(2)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1︰1和l︰2,写出原子个数比为1︰1的化合物的电子式 ,两种化合物可以任意比互溶,解释其主要原因为 。
(3)该配位化合物的化学式为 。
(4)A元素与B元素可形成分子式为A2B2的化合物,该化合物的分子具有平面结构,则其结构式为 ,用电子式表示化合物Na2D的形成过程 。

(5)已知E的晶胞结构如图所示,此晶胞立方体的边长为a cm,E单质的密度为ρ g·cm-3,则阿伏伽德罗常数为 (用a、ρ表示)。该晶胞配位数为 ,EDC4常作电镀液,其中DC42-的空间构型是 ,其中D原子的杂化轨道类型是 。若电解EDC4的水溶液,则电解总反应的化学方程式为 。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质对应的用途不正确的是( )
A |
| C | D | |
物质 | Fe2O3 | NH3 | Si | Na2O |
用途 | 作红色涂料 | 制硝酸 | 作半导体材料 | 作供氧剂 |


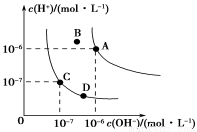
 关系为:KW(B)>KW(A)>KW(C)>KW(D)
关系为:KW(B)>KW(A)>KW(C)>KW(D) 合,溶液的pH=7
合,溶液的pH=7 CO2 (g) + H2 (g) K=1.0则一氧化碳在此反应条件下的转化率是 。
CO2 (g) + H2 (g) K=1.0则一氧化碳在此反应条件下的转化率是 。
 、Ba2+、AlO
、Ba2+、AlO 、Cl-
、Cl- 、Cl-
、Cl- B
B
 O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1,
O2(g)===Cu2O(s) ΔH=-169 kJ·mol-1, O2===CO(g) ΔH=-110.5 kJ·mol-1,
O2===CO(g) ΔH=-110.5 kJ·mol-1,
 4Cl溶液含NH4+物质的量不同
4Cl溶液含NH4+物质的量不同