��Ŀ����
����Ŀ����.������ Mg5Al3(OH)19(H2O)4 ������������ȼ���ϣ�����ʱ�����»�ѧ����ʽ�ֽ⣺2Mg5Al3(OH)19(H2O)4![]() 27H2O��+10MgO+3Al2O3
27H2O��+10MgO+3Al2O3
(1)д���û���������ȼ������������___________��
(2)�����ӷ���ʽ��ʾ��ȥ��������� Al2O3 ��ԭ��___________
(3)��֪ MgO������NH4Cl��ˮ��Һ���û�ѧ����ʽ��ʾ��ԭ��_____________��
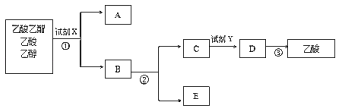
��.���Բ��� A(M=296g/mol)��������Ԫ����ɵĻ�������ij�о�С�鰴��ͼ����̽ ������ɣ�

��ش�
(4)A�Ļ�ѧʽΪ_____��C �гʻ�ɫ�����Ӷ�ӦԪ����Ԫ�����ڱ��е�λ��Ϊ__________��
(5)��֪������ A ����ϡ���ᷴӦ������һ�ֵ���ɫ�������һ������(����������������������ܶ�Ϊ2)����������ӵĵ���ʽΪ_____��д���÷�Ӧ�����ӷ���ʽ_________��
(6)д��F��G��Ӧ�Ļ�ѧ����ʽ____________��
���𰸡���Ӧ���Ƚ����¶����������������������ˮ����ϡ�Ϳ��� Al2O3 +2OH=2AlO2+H2O NH4Cl+H2O![]() NH3H2O+HCl��MgO+2HCl=MgCl2+H2O ��MgO+H2O+ 2NH4Cl=MgCl2+2NH3H2O Fe3S4 �������ڵ�����
NH3H2O+HCl��MgO+2HCl=MgCl2+H2O ��MgO+H2O+ 2NH4Cl=MgCl2+2NH3H2O Fe3S4 �������ڵ����� ![]() Fe3S4+6H+=3H2S��+3Fe2++S H2SO3+I2+H2O=H2SO4+2HI
Fe3S4+6H+=3H2S��+3Fe2++S H2SO3+I2+H2O=H2SO4+2HI
��������
����(1)�ֽⷴӦ�����ȷ�Ӧ�����ɵ�����þ�����������۵�ߣ�
(2)����þ�Ǽ����������������������������ݶ������ʲ�ͬ��ȥ��
(3)�Ȼ����Һ��笠�����ˮ����Һ�����ԣ�����þ������ٽ�ˮ��ƽ��������У�
����C����KSCN��DΪѪ��ɫ��Һ����֪CΪFeCl3��DΪFe(SCN)3�ȣ����ƿ�֪BΪFe2O3����n(Fe2O3)=![]() =0.03mol��n(Fe)=0.06mol��m(Fe)=0.06mol��56g/mol=3.36g��A�������ɵ���ɫ����E��Һˮ�õ�������Һ��������KI��Һ���õ���ɫ��ҺG��������Һ��������ǿ��˵���������E��ˮ��Һ��EӦΪSO2��FΪH2SO3��G���к�H2SO4��HI����֪A����Fe��SԪ�أ���m(S)=5.920g-3.36g=2.56g��n(S)=
=0.03mol��n(Fe)=0.06mol��m(Fe)=0.06mol��56g/mol=3.36g��A�������ɵ���ɫ����E��Һˮ�õ�������Һ��������KI��Һ���õ���ɫ��ҺG��������Һ��������ǿ��˵���������E��ˮ��Һ��EӦΪSO2��FΪH2SO3��G���к�H2SO4��HI����֪A����Fe��SԪ�أ���m(S)=5.920g-3.36g=2.56g��n(S)=![]() =0.08mol����֪n(Fe)��n(S)=3��4�����Դ˽�������
=0.08mol����֪n(Fe)��n(S)=3��4�����Դ˽�������
I.(1)2Mg5Al3(OH)19(H2O)4![]() 27H2O��+10MgO+3Al2O3���ֽⷴӦ�����ȷ�Ӧ���ή���¶ȣ��������ɵ�����þ�������������۵�ܸߵ���������ű������ֹȼ�գ�ˮ����ϡ�Ϳ���������������Ũ�ȣ�����������ȼ����
27H2O��+10MgO+3Al2O3���ֽⷴӦ�����ȷ�Ӧ���ή���¶ȣ��������ɵ�����þ�������������۵�ܸߵ���������ű������ֹȼ�գ�ˮ����ϡ�Ϳ���������������Ũ�ȣ�����������ȼ����
(2)����þ�Ǽ��������������ᣬ�����������������������ᡢ���ڼ�������������ܽ����˳�ȥ����Ӧ�����ӷ���ʽΪ��Al2O3+2OH-=2AlO2-+H2O��
(3)�Ȼ����Һ��笠�����ˮ����Һ�����ԣ�����þ����ˮ�����ɵ��ᣬ��Ӧ�Ļ�ѧ����ʽΪ��NH4Cl+H2O![]() NH3H2O+HCl��MgO+2HCl=MgCl2+H2O��MgO+2NH4Cl+H2O=MgCl2+2NH3H2O��
NH3H2O+HCl��MgO+2HCl=MgCl2+H2O��MgO+2NH4Cl+H2O=MgCl2+2NH3H2O��
II.C����KSCN��DΪѪ��ɫ��Һ����֪CΪFeCl3��DΪFe(SCN)3�ȣ���֪BΪFe2O3����n(Fe2O3)=![]() =0.03mol��n(Fe)=0.06mol��m(Fe)=0.06mol��56g/mol=3.36g��Aȼ�����ɵ���ɫ����E����ˮ�õ�������Һ��������KI��Һ���õ���ɫ��Һ������Һ������ǿ��˵���������E��ˮ��Һ��EӦΪSO2��FΪH2SO3��G���к�H2SO4��HI����֪A����Fe��SԪ�أ���m(S)=5.920g-3.36g=2.56g��n(S)=
=0.03mol��n(Fe)=0.06mol��m(Fe)=0.06mol��56g/mol=3.36g��Aȼ�����ɵ���ɫ����E����ˮ�õ�������Һ��������KI��Һ���õ���ɫ��Һ������Һ������ǿ��˵���������E��ˮ��Һ��EӦΪSO2��FΪH2SO3��G���к�H2SO4��HI����֪A����Fe��SԪ�أ���m(S)=5.920g-3.36g=2.56g��n(S)=![]() =0.08mol����֪n(Fe)��n(S)=3��4������AΪFe3S4��
=0.08mol����֪n(Fe)��n(S)=3��4������AΪFe3S4��
(4)�����Ϸ�����֪��AΪFe3S4�����е���Ԫ��λ��Ԫ�����ڱ��ĵ������� �ڢ�����
(5)������A����ϡ���ᷴӦ������һ�ֵ���ɫ�������һ�����壬����ɫ������ΪS���������Է�������ΪNH3��2������Է���������17��2=34��ΪH2S���壬�����ʽΪ![]() ����Ӧ�����ӷ���ʽΪFe3S4+6H+=3Fe2++S+3H2S����
����Ӧ�����ӷ���ʽΪFe3S4+6H+=3Fe2++S+3H2S����
(6)I2�������ԣ�����Һ�н�H2SO3����Ϊ���ᣬ����F��G��Ӧ�Ļ�ѧ����ʽΪH2SO3+I2+H2O=H2SO4+2HI��

 �ŵ������ϵ�д�
�ŵ������ϵ�д�