��Ŀ����
����Ŀ��A��B��C��D��E���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶D��C��A��E��B������A��B����ͬһ���ڣ�A��C����ͬһ���壮Cԭ�Ӻ�������������A��Bԭ�Ӻ���������֮�ͣ�Cԭ��������ϵĵ�������Dԭ��������������4������DΪ�������Իش�
��1��C��Ԫ������Ϊ ��
��2��������Ԫ���У����γɵ����Һ̬����̬�⻯����ȶ����ɴ�С��˳����
��3��A��B�γɵ���ԭ�ӷ��ӵĽṹʽ�� �� B��D�γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����ĵ���ʽ�� ��
��4����д��һ��������5��Ԫ���в���Ԫ���γɵ����ʣ������û���Ӧ����ʽ ��
���𰸡�
��1����
��2��H2O��NH3
��3��O=C=O��![]()
��4��2C+SiO2 ![]() 2CO��+Si
2CO��+Si
���������⣺A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶D��C��A��B������A��B����ͬһ���ڣ�A��C����ͬһ���壬����Ԫ�������ڱ��еĴ������λ��Ϊ�� ![]() ��A��C����ͬһ���壬�������������8��Cԭ�Ӻ�������������A��Bԭ�Ӻ���������֮�ͣ���B��������Ϊ8����BΪOԪ�أ�Cԭ��������ϵĵ�������Dԭ��������������4������C����������Ϊ4��D������������Ϊ1����AΪCԪ�أ�CΪSiԪ�أ�DΪNaԪ�أ�E��ԭ�Ӱ뾶����B��O����С��A��̼������EΪNԪ��.
��A��C����ͬһ���壬�������������8��Cԭ�Ӻ�������������A��Bԭ�Ӻ���������֮�ͣ���B��������Ϊ8����BΪOԪ�أ�Cԭ��������ϵĵ�������Dԭ��������������4������C����������Ϊ4��D������������Ϊ1����AΪCԪ�أ�CΪSiԪ�أ�DΪNaԪ�أ�E��ԭ�Ӱ뾶����B��O����С��A��̼������EΪNԪ��.
��1.��CΪSiԪ�أ����Դ��ǣ��裻
��2.���ǽ�����O��N��C��Si�����⻯����ȶ���ΪH2O��NH3��CH4��SiH4 �� ���Դ��ǣ�H2O��NH3��CH4��SiH4��
��3.��A��B�γɵ���ԭ�ӷ���ΪCO2 �� ��ṹʽΪO=C=O��B��D�γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����ΪNa2O2 �� ����ʽ�� ![]() �����Դ��ǣ�O=C=O��
�����Դ��ǣ�O=C=O�� ![]() ��
��
��4.��������Ϣ����д����Ӧ2C+SiO2 ![]() 2CO��+Si�����Դ��ǣ�2C+SiO2
2CO��+Si�����Դ��ǣ�2C+SiO2 ![]() 2CO��+Si��
2CO��+Si��

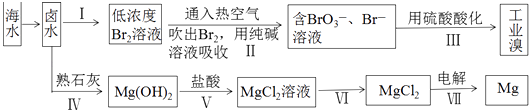
 �»����ܶ�Ա��ϵ�д�
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�