题目内容
【题目】(1)下列微粒中,只有氧化性的是_____________ (用字母填写,下同),既有氧化性又有还原性的是___________________。
A. Cl2 B. S2— C. H+ D. Na E. FeCl2
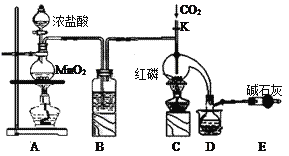
(2)在4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O反应中
MnCl2+Cl2↑+2H2O反应中
①氧化剂是________,氧化产物是________;
②被氧化与未被氧化的HCl的质量之比为_______,若有7.3gHCl被氧化,转移电子的物质的量为________;。
【答案】C AE MnO2 Cl2 1:1 0.2mol
【解析】
当元素在化合物中处于最高化合价时,只有氧化性,处于最低化合价时,只有还原性,处于中加价态时,既有氧化性又有还原性;在4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O反应中盐酸既表现了还原性又表现了酸性,所以,要按实际参加氧化还原反应的HCl分析。
MnCl2+Cl2↑+2H2O反应中盐酸既表现了还原性又表现了酸性,所以,要按实际参加氧化还原反应的HCl分析。
(1) 氢元素的化合价有-1、0、+1 ,而H+是+1价,处于最高价,所以H+只有氧化性,S2、Na处于最低价只有还原性; Cl2中Cl的化合价为0价、 FeCl2中的Fe为+2价 ,均为中间价态,所以既有氧化性又有还原性。故答案为C; AE ;
(2)①在4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O反应中, Mn由+4价变成了+2价,化合价降低,所以MnO2,是氧化剂, Cl由-1价变成了0价,化合价升高,所以Cl2是氧化产物,故答案为MnO2; Cl2
MnCl2+Cl2↑+2H2O反应中, Mn由+4价变成了+2价,化合价降低,所以MnO2,是氧化剂, Cl由-1价变成了0价,化合价升高,所以Cl2是氧化产物,故答案为MnO2; Cl2
②从方程式中可以看出,被氧化的HCl和未被氧化的HCl , 物质的量之比为1:1 ,所以质量之比为1:1 ; 7.3g的HCl为0.2mol,设有7.3gHCl被氧化,转移电子的物质的量为x则有2:2=0.2 : x, x=0.2mol ,故答案为1:1 ; 0.2mol。