题目内容
【题目】下列叙述正确的是( )
A.1molH2O的质量为18g/mol
B.摩尔是国际单位制中的一个基本物理量
C.3.01×1023个SO2分子的质量为32g
D.C2H5OH的摩尔质量为46g
【答案】C
【解析】
A. 1mol水的质量为18g,g/mol为摩尔质量的单位,A错误;
B. 摩尔质量是物质的量的单位,而不是物理量,B错误;
C. 3.01×1023个SO2分子的物质的量为0.5mol,质量为0.5mol×64g/mol=32g,C正确;
D. C2H5OH的摩尔质量为46g/mol,g为质量的单位,D错误;
故答案选C。

练习册系列答案
相关题目
【题目】在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )
A.所用NaOH已经潮解B.有少量NaOH溶液残留在烧杯里
C.向容量瓶中加水未到刻度线D.称量时误用“左码右物”
【题目】镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有________。
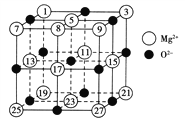
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:__________________。
(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1 266 | 1 534 | 183 |
解释表中氟化物熔点差异的原因:_____________________________________。