题目内容
在体积不变的密闭容器中,2NO2(g)  N2O4(g) 达到平衡的标志是
N2O4(g) 达到平衡的标志是
①消耗1 mol NO2的同时消耗1 mol N2O4 ②容器内NO2 和N2O4的物质的量相等
③混合气体的颜色不再改变 ④容器内NO2的物质的量浓度不再变化
| A.①② | B.①②③ | C.③④ | D.①③④ |
C
解析试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项④正确。颜色的深浅和浓度有关系,混合气体的颜色不再改变,说明NO2的浓度不再发生变化,所以选项③可以说明。①中反应速率的方向相反,但不能满足速率之比是相应的化学计量数之比,不能说明。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,②不能说明,因此答案选C。
考点:考查可逆反应平衡状态的判断
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。

 名校课堂系列答案
名校课堂系列答案一定条件下,化学反应方向的判据为:△G=△H-T△S。已知反应A(s)= D(g)+E(g),△H-T△S=(-4499+11T)J/mol,(温度单位为K)。要防止A分解反应发生,温度必须( )
| A.高于或等于409K | B.低于136K |
| C.高于136K而且低于409K | D.任意温度 |
可逆反应2NO2 2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2,NO,O2表示的反应速率的比为2:2:1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
| A.①④⑥⑦ | B.②③⑤⑦ | C.①③④⑤ | D.全部 |
下列有关化学反应速率和限度的说法中,不正确的是( )
| A.实验室用H2O2分解制O2,加入MnO2后,反应速率明显加快 |
| B.在金属钠与足量水反应中,增加水的量能加快反应速率 |
C.2SO2+O2 2SO3,反应中,SO2不能全部转化为SO3 2SO3,反应中,SO2不能全部转化为SO3 |
| D.实验室用碳酸钙和盐酸反应抽取CO2,用碳酸钙粉末比块状碳酸钙反应要快 |
在一定条件下,反应N2 + 3H2 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7 g,则反应速率为
| A.v(H2)="0.03" mol/(L·min) | B.v(N2)="0.02" mol/(L·min) |
| C.v(NH3)="0.01" mol/(L·min) | D.v(NH3)="0.17" mol/(L·min) |
反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
| A.0.1s | B.2.5s | C.5s | D.10s |

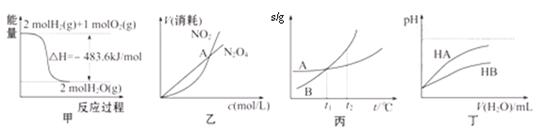
 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是 ( )
2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是 ( )