��Ŀ����
����Ŀ����������(NOCl)�����ںϳ�����������������һ�������ڳ��³�ѹ�ºϳɡ��۵㣺-64.5�棬�е㣺-5.5��;�������ǻ�ɫ���ж����壬��ˮ��ˮ�⡣��֪NO����NaOH��Һ��Ӧ���밴Ҫ��ش��������⡣
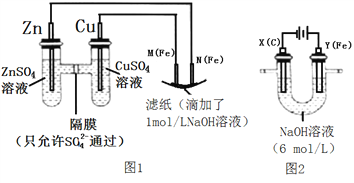
(1)������м��ϡ�����ַ�Ӧ�Ʊ�NO�����ӷ���ʽΪ_____________������������ͬ��ѡ����Ƭ��ͭƬ�Ʊ�NO���ŵ���_______________��
(2)�Ʊ�NOCl��װ������ͼ��ʾ������˳��Ϊa��_______________(�������������ҷ�����Сд��ĸ��ʾ��

��װ��A�з�Ӧ�Ļ�ѧ����ʽ��_______________��NOCl�����и�ԭ�Ӿ�����8�����ȶ��ṹ�������ĵ���ʽΪ_______________��
����ʵ����û�а�װװ��B��������_______________��
��ʵ�鿪ʼӦ����װ����ͨ��Cl2����װ��A�г�������ɫ����ʱ���ٽ�NO����ͨ�룬�˲�����Ŀ����_______________��
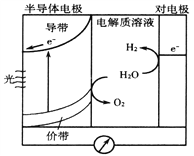
(3)��ҵ����������NOβ�����������ж��֣����м�ӵ绯ѧ������ԭ����ͼ��ʾ��

���������ڷ����ķ�ӦΪ_______________��
�������ĵ缫��ӦʽΪ_______________��
���𰸡� 3Fe+8H++2NO3-=3Fe2++2NO��+4H2O ��ͬ�����£�������NO ��ͭ�� e��f(��f��e)��c��b��d Cl2+2NO==2NOCl ![]() ˮ�������뷴Ӧ�������NOCl ˮ�� ����װ���п�������ֹ�����е�O2 ��NO ��Ӧ 2NO+2S2O42+2H2O=N2+4HSO3 2HSO3+ 2H+ + 2e= S2O42+ 2H2O
ˮ�������뷴Ӧ�������NOCl ˮ�� ����װ���п�������ֹ�����е�O2 ��NO ��Ӧ 2NO+2S2O42+2H2O=N2+4HSO3 2HSO3+ 2H+ + 2e= S2O42+ 2H2O
�����������������(1) ������м��ϡ�����ַ�Ӧ��������������һ��������ˮ����ͬ������������NO�����ͭ�ࣻ(2) ������һ��������A������NOCl��NOCl�е㣺-5.5���������ñ���ˮ�ռ�NOCl��NOCl��ˮ��ˮ����Ϊ��ֹNOClˮ������β������ǰ���Ӹ���װ���� NO���� O2��Ӧ����NO2��(3) �ٸ���ͼʾ����������NO��S2O42��Ӧ����N2��HSO3��������HSO3�õ�������S2O42��
������(1) ������м��ϡ�����ַ�Ӧ��������������һ��������ˮ����Ӧ���ӷ���ʽ��3Fe+8H++2NO3-=3Fe2++2NO��+4H2O��ѡ����Ƭ��ͭƬ�Ʊ�NO���ŵ��ǣ���ͬ������������NO�����ͭ�ࣻ(2) ������һ��������A������NOCl��NOCl�е㣺-5.5���������ñ���ˮ�ռ�NOCl��NOCl��ˮ��ˮ����Ϊ��ֹNOClˮ������β������ǰ���Ӹ���װ������������˳����e��f(��f��e)��c��b��d����װ��A��������һ��������Ӧ����NOCl����ѧ����ʽ��Cl2+2NO==2NOCl��NOCl�����и�ԭ�Ӿ�����8�����ȶ��ṹ�����ݳɼ�����������ʽΪ![]() ����NOCl��ˮ��ˮ������ʵ����û�а�װװ��B��ˮ�������뷴Ӧ�������NOCl ˮ������ʵ�鿪ʼӦ����װ����ͨ��Cl2����װ��A�г�������ɫ����ʱ���ٽ�NO����ͨ�룬���Է�ֹ��ֹ�����е�O2 ��NO ��Ӧ�� (3) �ٸ���ͼʾ����������NO��S2O42��Ӧ����N2��HSO3����Ӧ���ӷ���ʽ��2NO+2S2O42+2H2O=N2+4HSO3��������HSO3�õ�������S2O42��������Ӧʽ��2HSO3+ 2H+ + 2e= S2O42+ 2H2O��
����NOCl��ˮ��ˮ������ʵ����û�а�װװ��B��ˮ�������뷴Ӧ�������NOCl ˮ������ʵ�鿪ʼӦ����װ����ͨ��Cl2����װ��A�г�������ɫ����ʱ���ٽ�NO����ͨ�룬���Է�ֹ��ֹ�����е�O2 ��NO ��Ӧ�� (3) �ٸ���ͼʾ����������NO��S2O42��Ӧ����N2��HSO3����Ӧ���ӷ���ʽ��2NO+2S2O42+2H2O=N2+4HSO3��������HSO3�õ�������S2O42��������Ӧʽ��2HSO3+ 2H+ + 2e= S2O42+ 2H2O��