题目内容
有关热化学方程式书写与对应表述均正确的是( )
A. 已知2C(s)+O2(g)=2CO(g) △H=-221 kJ·mol-1, 则可知C的标准燃烧热为110.5 kJ·mol-1
B. 在101KPa下氢气的标准燃烧热△H =-285.5 kJ·mol则水分解的热化学方程式: 2H2O(l)=2H2(g)+O2(g) △H = +285.5 kJ·mol-1
C. 稀硫酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq) = H2O(l) △H = -57.3 kJ·mol-1
D. 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量。则Fe(s)+S(g)=FeS(s) △H= - 95.6 kJ·mol-1
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。

Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_____g。
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol):_____________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H=______________取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是:______。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度


 xC(g),符合图Ⅰ所示关系。对图Ⅱ的说法正确的是(T为温度、P为压强、t为时间) ( )
xC(g),符合图Ⅰ所示关系。对图Ⅱ的说法正确的是(T为温度、P为压强、t为时间) ( )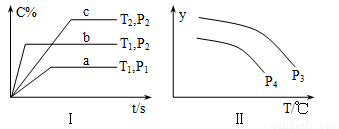
 ),简称AAPP,常用作染料、有机颜料中间体。其合成路线如下:
),简称AAPP,常用作染料、有机颜料中间体。其合成路线如下: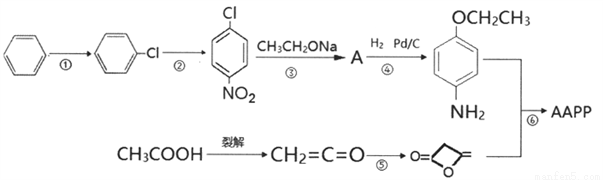
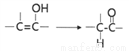
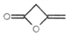 有多种同分异构体,写出三种符合下列要求的同分异构体_________
有多种同分异构体,写出三种符合下列要求的同分异构体_________