题目内容
【题目】Ⅰ.某化合物A由两种元素组成,可以发生如下的转化。
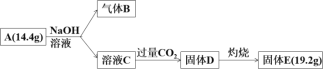
已知:标准状况下,气体B的密度是氢气的8倍。请回答:
(1)组成A的元素有_________,A的化学式是_________
(2)请写出A与NaOH溶液反应的化学方程式_________
(3)A可用于金属的冶炼,请写出A与Fe2O3的化学反应方程式_________
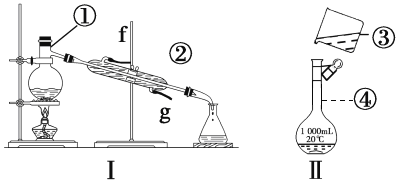
Ⅱ.某实验小组做了如下实验:

请回答:
(1)写出硬质管中发生反应的化学方程式:_________
(2)有同学认为乙醇的催化氧化反应产物中含有乙酸,请设计实验检验产物成分:_____。
【答案】Al、C Al4C3 Al4C3+4NaOH+4H2O=3CH4↑+4NaAlO2 Al4C3+4Fe2O3=2Al2O3+8Fe+3CO2↑ CH3CH2OH+CuO=CH3CHO+Cu+H2O 将产生的气体分别通入两份新制氢氧化铜悬浊液中,标为A、B,对B进行加热,若A沉淀溶解,B出现砖红色沉淀,则既有乙酸也有乙醛;若A沉淀溶解,B无砖红色沉淀,则只有乙酸;若A沉淀不溶解,B出现砖红色沉淀,则只有乙醛
【解析】
Ⅰ.已知标准状况下,气体B的密度是氢气的8倍,则气体B的摩尔质量为16g/mol,应为CH4气体,则A中含有C元素,同时A能与氢氧化钠溶液反应,则A中含有Al元素,A为Al4C3,C为NaAlO2,NaAlO2溶液中通入过量二氧化碳得到D为氢氧化铝固体,进一步灼烧得到E为氧化铝,据此分析解答;
Ⅱ.(1)乙醇被CuO氧化,反应生成乙醛、铜单质和水;
(2)根据乙酸和乙醛与新制氢氧化铜悬浊液反应现象的不同分析比较。
Ⅰ. (1)由以上分析知,组成A的元素有Al、C,A的化学式是Al4C3,故答案为:Al、C;Al4C3;
(2)Al4C3与NaOH溶液反应生成CH4和4NaAlO2,故反应的化学方程式为Al4C3+4NaOH+4H2O=3CH4↑+4NaAlO2;
(3)Al4C3可用于金属的冶炼,其与Fe2O3反应生成Al2O3、Fe和CO2,故反应的化学反应方程式为Al4C3+4Fe2O3=2Al2O3+8Fe+3CO2↑;
Ⅱ.(1)乙醇被CuO氧化,反应生成乙醛、铜单质和水,反应的化学方程式为CH3CH2OH+CuO=CH3CHO+Cu+H2O;
(2)根据乙酸和乙醛性质的区别,可将产生的气体分别通入两份新制氢氧化铜悬浊液中,标为A、B,对B进行加热,若A沉淀溶解,B出现砖红色沉淀,则既有乙酸也有乙醛;若A沉淀溶解,B无砖红色沉淀,则只有乙酸;若A沉淀不溶解,B出现砖红色沉淀,则只有乙醛。