题目内容
晶体具有规则的几何外形,晶体中最基本的重复单位被称为晶胞。中学教材中NaCl晶体结构即为NaCl的一个晶胞。已知FexO晶体的晶胞结构为NaCl型,由于晶体缺陷,x<1。实验测得FexO晶体的密度为5.71g/cm3,晶胞的边长为4.28×10-5m。NaCl的晶胞如图所示:
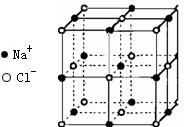
(1)求FexO中X的具体数值(精确至0.01)为 ,晶体中Fe元素只有+2和+3价,则在Fe2+、Fe3+ 的总数中,Fe2+所占分数(用小数表示,精确至0.001)为
(2)此晶体的化学式为
(3)晶体中与O2-距离最近且相等的Fe2+或Fe3+所围成的几何构形是
 (4)晶体中,Fe离子间最近距离为 cm
(4)晶体中,Fe离子间最近距离为 cm

(1)求FexO中X的具体数值(精确至0.01)为 ,晶体中Fe元素只有+2和+3价,则在Fe2+、Fe3+ 的总数中,Fe2+所占分数(用小数表示,精确至0.001)为
(2)此晶体的化学式为
(3)晶体中与O2-距离最近且相等的Fe2+或Fe3+所围成的几何构形是
 (4)晶体中,Fe离子间最近距离为 cm
(4)晶体中,Fe离子间最近距离为 cm1)0.92 , 0.826 (各1分)
2 Fe2+0.76 Fe3+0.16O ( 2分)
3)正八面体 ( 2分)
4)3.03×10-8 ( 2分)
2 Fe2+0.76 Fe3+0.16O ( 2分)
3)正八面体 ( 2分)
4)3.03×10-8 ( 2分)
NaCl型,每个晶胞中含有4个“NaCl”。模仿NaCl,先求摩尔体积,再求摩尔质量。
Vm=(4.28×10―8) 3×NA/4 cm3·mol-1
M=5.719×Vm g·mol-1=67.48g·mol-1
⑴x=(67.48-16)/55.9=0.92
⑵根据电荷守恒,或化合价代数和为0,求出Fe2+(a)与Fe3+(b)。
2a+3b=2
a+b=0.92
得a=0.76
b=0.16
0.76/0.92=0.826即82.6%
⑶正八面体(参见NaCl晶体图)
⑷设Fe在面心,另外的正方形的四个顶点(参见NaCl晶体)
则:求对角线的一半即为最短距离。
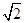 ×(4.28×10―10)/2 m=3.03×10―10m==3.03×10―8cm
×(4.28×10―10)/2 m=3.03×10―10m==3.03×10―8cm
练习册系列答案
相关题目

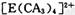 配离子,其中存在的化学键类型有 ______ (填序号);
配离子,其中存在的化学键类型有 ______ (填序号);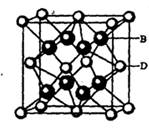
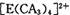 具有对称的空间构型,且当
具有对称的空间构型,且当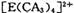 中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则
中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则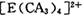 的空间构型为 ____________ (填序号);
的空间构型为 ____________ (填序号);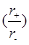 不相等,所以两晶体中离子的配位数不相等
不相等,所以两晶体中离子的配位数不相等 晶 ④水银 ⑤氧化铝 ⑥P4 ⑦苯
晶 ④水银 ⑤氧化铝 ⑥P4 ⑦苯 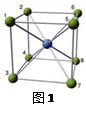
 宏观外形为 。
宏观外形为 。
 晶体一定是分子晶体 ⑥.元素周期表从ⅢB族到ⅡB族8个纵行的元素都是金属元素 ⑦.在 SiO2和干冰晶体中,都存在单个分子
晶体一定是分子晶体 ⑥.元素周期表从ⅢB族到ⅡB族8个纵行的元素都是金属元素 ⑦.在 SiO2和干冰晶体中,都存在单个分子 属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是 ( )
属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是 ( )