��Ŀ����
����Ŀ���ѻӷ��Զ����㣨TaS2���ɲ�������װ���ᴿ����������TaS2��ĩװ��ʯӢ��һ�ˣ�����պ����������Ⲣ��ܣ����ڼ���¯�У���Ӧ���£�TaS2��s��+2I2��g��TaI4��g��+S2��g������˵����ȷ���ǣ� �� ![]()
A.�ڲ�ͬ�¶�����TaI4�������ֲ���
B.���ᴿ�����У�I2�������ϼ���
C.���ᴿ�����У�I2�������ǽ�TaS2�Ӹ�����ת�Ƶ�������
D.�÷�Ӧ��ƽ�ⳣ����TaI4��S2��Ũ�ȳ˻��ɷ���
���𰸡�C
���������⣺A�����ݷ�Ӧ������֪���¶Ȳ�ͬʱ��Ӧ���е���Ҫ����ͬ��TaI4�����ı䣬��A����
B����Ϊ����ͬһ�ܱ�ϵͳ���������غ㶨�ɿ�֪I2���������ܲ��ϼ��٣���һ�������´ﵽƽ����ٱ仯����B����
C�����ᴿ�����У�I2�������dz䵱һ�������˹����Ľ�ɫ����TaS2�Ӹ�����ת�Ƶ��������Դﵽ�ᴿ��Ŀ�ģ���C��ȷ��
D������ƽ�ⳣ������ʽ��֪��ƽ�ⳣ����ƽ��ʱ�������Ũ���ݴη��˻����Է�Ӧ��ƽ��Ũ�ȵ��ݴη��˻�������ƽ�ⳣ��K��Tal4��S2��Ũ�ȳ˻������ȣ���D����
��ѡC��
Ӧ�������Ϣ�еĻ�ѧƽ�⣬���ƽ������ۺ�֪ʶ���з����жϣ�TaS2��s��+2I2��g��TaI4��g��+S2��g���ǻ�ѧƽ�⣬�����㣨TaS2�����ѻӷ������ʣ����ͼʾ�ж������λ�ÿ�֪���ᴿ�ǰѶ����㣨TaS2���͵ⵥ���ڸ����·�Ӧ��������TaI4��g����S2��g�������Ը÷�Ӧ����Ӧ�����ȷ�Ӧ����������ɢ����������ƽ���������ɶ����㣨TaS2����I2��g����ʹ�����㣨TaS2���õ��ᴿ��

 �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�����Ŀ����ͼa��b��c��d��Ϊ���缫����ѡ��ĵ������Һ���±���
�� | A | B | C | D |
�ײ� | NaOH | Cu��N O3��2 | KCl | Na2SO4 |
�Ҳ� | CuSO4 | NaCl | AgNO3 | NaNO3 |
Ҫ����������ǣ��ٹ���һ��ʱ��ײ۵��ҺpH���������Ҳ۵��ҺpH�½�����b��c�����ŵ����ӵ����ʵ�����ȣ���Ӧѡ�õĵ��Һ�ǣ� ��
A.A
B.B
C.C
D.D
����Ŀ������ͭ��һ��Ӧ�ü���㷺�Ļ���ԭ�ϣ�������ij�����ú�����ͭΪԭ������������CuSO45H2O������������ʾ��ͼ�� 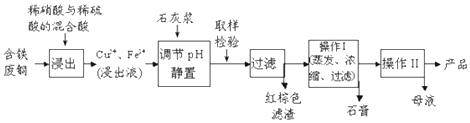
������ʯ���ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ��������
�¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
ʯ�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
���� | 32 | 44.6 | 61.8 | 83.8 | 114 |
��ش��������⣺
��1������ɫ��������Ҫ�ɷ�����
��2��д��������������������ͭ�Ļ�ѧ����ʽ��
��3������I�IJ����¶�Ӧ�ÿ����������ң�
��4������Һ�з��������ͭ����IJ���IIӦΪϴ�ӡ����
��5����Ӧ�����е�NO����ѭ��ʹ�ã��Խ���һ����ѧ����ʽ��ʾNOת��ΪHNO3��
����Ŀ��������Һ����ε��뵽���У���ͼ����ʵ������Ԥ�������һ�µ��ǣ� ��
ѡ�� | �������� | �������� | Ԥ����е����� |
A | ��ˮ | �Ȼ�����Һ | ������ɫ���� |
B | Ũ���� | ͭƬ | ��������������Һ���� |
C | Ũ���� | ��ɰֽ��ĥ�������� | ������������ɫ���� |
D | ϡ���� | Na2CO3��NaOH�Ļ��Һ | ���������������� |
A.A
B.B
C.C
D.D