��Ŀ����
| |||||||||||
������
(1) |
�¶ȸ���35��,̼����炙�ֽ� |
(2) |
ʹ��Ӧ��ֽ���,��ͬ�¶��£�̼�����Ƶ��ܽ����С,NaCl��NH4Cl��NH4HCO3 |

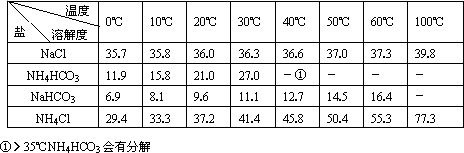
| ���� | 0�� | 10�� | 20�� | 30�� | 40�� | 50�� | 60�� | 100�� |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | 35�����Ϸֽ� | |||
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
| A����һ��������Ӧ�Ļ�������Ϊ���Ϸ�Ӧ���ֽⷴӦ |
| B����һ��������Ӧ֮�����Ҫʵ������ǹ��ˡ�ϴ�� |
| C����һ����Ӧ�����¶ȸ���30��Ŀ������߷�Ӧ���� |
| D����ӦҺ�����ᴦ����ʹNaClѭ��ʹ�ò�����NH4Cl |
1942�꣬�ҹ�����ר�Һ�°���NaCl��NH3��CO2��Ϊԭ�����Ƶ�NaHCO3�����������˴���������Ƽ��Ϊ�����Ƽҵ������ͻ�����ס��йط�Ӧ�Ļ�ѧ����ʽ���£�
������ NH3+CO2+H2O=NH4HCO3��NH4HCO3+NaCl=NaHCO3��+NH4Cl;
�������� 2NaHCO3=Na2CO3+CO2��+H2O
�� ��1���������Ƽ���Ѻϳɰ��ʹ������ֲ�Ʒ������������֪�ϳɰ�Ϊ���ȷ�Ӧ������������Ѯԭ�����������ϳɰ�Ӧѡ����¶Ⱥ�ѹǿ���������� ��ѡ����ĸ����
������ a.���¡� b.���¡� c.���¡� d.��ѹ�� e.��ѹ�� f.��ѹ
�� ��2��̼������뱥��ʳ��ˮ��Ӧ��������̼�����ƾ����ԭ������������ ��ѡ����ĸ��
������ a.̼������������ˮ
������ b.̼�����������ֽ�
���� �� c.̼�����Ƶ��ܽ����Խ�С����������Һ�����Ƚᾧ����
�� ��3��ij̽���С����� �����Ƽ�ԭ�������Ʊ�̼�����ƣ�ͬѧ�ǰ�������Ƶķ�������ʵ�顣
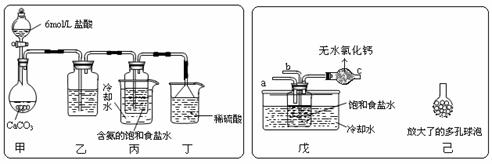
��һλͬѧ����������̼����ͨ�뺬���ı���ʳ��ˮ���Ʊ�̼�����ƣ�ʵ��װ������ͼ��ʾ��ͼ�мг֡��̶��õ�����δ��������
|
�ڶ�ͬѧ����ͼ����װ�ý���ʵ�飨����װ��δ��������
Ϊ��߶�����̼�ڴ˷�Ӧ��Һ�б����յij̶ȣ�ʵ��ʱ�����ȴ�a��ͨ������ ���壬�ٴ�b����ͨ���������� ���塣
�� ��4��������д��һ��ʵ������ȡ����̼�����Ƶķ���������صĻ�ѧ��Ӧ����ʽ�������������������������������������������������������������������� ��