题目内容
【题目】现有下列反应:
①、2H2O+Cl2+SO2=H2SO4+2HCl
②、 KMnO4+ HCl(浓)= KCl+__MnCl2+___Cl2↑+___H2O
针对上述两个反应回答:
(1)配平②的化学方程式________;
(2)用单线桥标出①中电子转移的方向和数目________;
(3)Cl2、SO2和KMnO4的氧化性强弱顺序为____;
(4)反应①中氧化产物和还原产物的物质的量之比为___;
(5)反应②中氯化氢表现出的性质是___。
A.还原性 B.酸性 C.氧化性
【答案】 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O 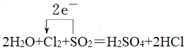 KMnO4 >Cl2>SO2 1:2 ab
KMnO4 >Cl2>SO2 1:2 ab
【解析】(1)Mn元素化合价从+7价降低到+2价,得到5个电子。氯元素化合价从-1价升高到0价,失去1个电子,根据电子得失守恒和原子守恒可知反应②的化学方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O;(2)反应①中氯元素化合价从0价降低到-1价,S元素化合价从+4价升高到+6价,因此转移2个电子,则用单线桥表示①中电子转移的方向和数目为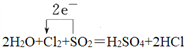 ;(3)氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,则根据反应的方程式可知Cl2、SO2和KMnO4的氧化性强弱顺序为KMnO4 >Cl2>SO2;(4)反应①中氧化产物和还原产物分别是硫酸和氯化氢,物质的量之比为1:2;(5)反应②中还有氯化锰生成,所以氯化氢表现出的性质除了还原性以外还有酸性,答案选ab。
;(3)氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性,则根据反应的方程式可知Cl2、SO2和KMnO4的氧化性强弱顺序为KMnO4 >Cl2>SO2;(4)反应①中氧化产物和还原产物分别是硫酸和氯化氢,物质的量之比为1:2;(5)反应②中还有氯化锰生成,所以氯化氢表现出的性质除了还原性以外还有酸性,答案选ab。

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
