题目内容
用惰性电极电解一定量的硫酸铜溶液,电解一段时间后,向电解液加入0.1mol碱式碳酸铜晶体(不含结晶水),恰好使溶液恢复到电解前的浓度和pH.下列有关叙述不正确的是( )
分析:电解硫酸铜溶液后溶液呈酸性,向电解后的溶液中加入碱式碳酸铜能恢复原溶液,碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,溶液质量增加的量是铜、氢氧根离子,所以实际上电解硫酸铜溶液分两个阶段:
第一阶段2CuSO4+2H2O
2Cu↓+O2↑+2H2SO4,
第二阶段:2H2O
2H2↑+O2↑,
将碱式碳酸铜化学式改变为2CuO?H2O?CO2,所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,根据氧化铜和水的量计算即可.
第一阶段2CuSO4+2H2O
| ||
第二阶段:2H2O
| ||
将碱式碳酸铜化学式改变为2CuO?H2O?CO2,所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,根据氧化铜和水的量计算即可.
解答:解:电解硫酸铜溶液后溶液呈酸性,向电解后的溶液中加入碱式碳酸铜能恢复原溶液,碱式碳酸铜和硫酸反应生成硫酸铜、水和二氧化碳,溶液质量增加的量是铜、氢氧根离子,所以实际上电解硫酸铜溶液分两个阶段:
第一阶段2CuSO4+2H2O
2Cu↓+O2↑+2H2SO4,
第二阶段:2H2O
2H2↑+O2↑,
将碱式碳酸铜化学式改变为2CuO?H2O?CO2,所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,
第一阶段:根据铜原子守恒知,电解硫酸铜溶液析出n(Cu)=n(CuO)=0.2mol,转移电子的物质的量=0.2mol×2=0.4mol;
第二阶段:电解生成0.1mol水转移电子的物质的量=0.1mol×2=0.2mol,
所以解过程中共转移的电子数为0.4mol+0.2mol=0.6mol;
A、电解分为两步电解硫酸铜和水生成氧气0.1mol,电解0.1mol水生成0.1mol氢气和0.05mol氧气,共生成气体0.15mol+0.1mol=0.25mol,气体标准状况体积=0.25mol×22.4L/mol=5.6L,故A正确;
B、上述分析计算可知电子转移总数为0.6mol,电解过程转移的电子数=0.6mol×6.02×1023=3.612×1023个,故B正确;
C、电解硫酸铜溶液分两个阶段:第一阶段2CuSO4+2H2O
2Cu↓+O2↑+2H2SO4,第二阶段:2H2O
2H2↑+O2↑,故C错误;
D、加入的碱式碳酸铜的反应是:Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3H2O,故D正确;
故选C.
第一阶段2CuSO4+2H2O
| ||
第二阶段:2H2O
| ||
将碱式碳酸铜化学式改变为2CuO?H2O?CO2,所以加入0.1molCu2(OH)2CO3 就相当于加入0.2molCuO和0.1mol水,
第一阶段:根据铜原子守恒知,电解硫酸铜溶液析出n(Cu)=n(CuO)=0.2mol,转移电子的物质的量=0.2mol×2=0.4mol;
第二阶段:电解生成0.1mol水转移电子的物质的量=0.1mol×2=0.2mol,
所以解过程中共转移的电子数为0.4mol+0.2mol=0.6mol;
A、电解分为两步电解硫酸铜和水生成氧气0.1mol,电解0.1mol水生成0.1mol氢气和0.05mol氧气,共生成气体0.15mol+0.1mol=0.25mol,气体标准状况体积=0.25mol×22.4L/mol=5.6L,故A正确;
B、上述分析计算可知电子转移总数为0.6mol,电解过程转移的电子数=0.6mol×6.02×1023=3.612×1023个,故B正确;
C、电解硫酸铜溶液分两个阶段:第一阶段2CuSO4+2H2O
| ||
| ||
D、加入的碱式碳酸铜的反应是:Cu2(OH)2CO3+2H2SO4═2CuSO4+CO2↑+3H2O,故D正确;
故选C.
点评:本题考查了电解原理,明确实际上加入的物质是解本题关键,再根据原子守恒、转移电子守恒来分析解答,难度中等

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
用惰性电极电解一定量的硫酸铜溶液,实验装置如下图甲.电解过程中的实验数据如下图乙,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).则下列说法中不正确的是( )


| A、电解过程中,a电极表面先有红色物质析出,后有气泡产生 | ||||
B、b电极上发生的反应方程式为4OH--4e-
| ||||
| C、曲线O~P段表示H2的体积变化 | ||||
| D、Q点时收集到的混合气体中H2和O2体积比为1:1 |

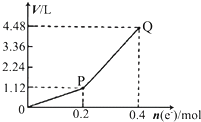 用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )