题目内容
【题目】在120℃、101kPa条件下,由H2、CH4组成的混合气体amL,通入一定量(设为xmL)氧气使其完全燃烧。
(1)若amL混合气体完全燃烧消耗相同条件下氧气的体积也为amL(即x=a),则原混合气体中CH4的体积分数是_____(保留三位有效数字);
(2)若原混合气体完全燃烧时,生成的气体中只有CO2和H2O(g),则x的取值范围是______。
【答案】33.3% 0.5a<x<2a
【解析】
(1)燃烧发生反应:2H2+O2=2H2O(g)、CH4+2O2=CO2+2H2O(g),假设甲烷为y mL,则氢气为(a-y)mL,根据方程式表示出各自消耗氧气的体积,进而列方程计算解答;
(2)由方程式可知,全部为氢气消耗氧气最小,全部为甲烷消耗氧气最多,据此讨论计算解答。
(1)假设甲烷为ymL,则氢气为(ay)mL,则:

由题意可知,2ymL+0.5(ay)mL=amL,解得y=![]() a,即甲烷的体积分数为
a,即甲烷的体积分数为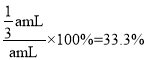
(2)全部为氢气消耗氧气最小,由2H2+O2=2H2O(g),可知消耗氧气为0.5amL,全部为甲烷消耗氧气最多,由CH4+2O2=CO2+2H2O(g),可知消耗氧气为2amL,故0.5a<x<2a。

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目