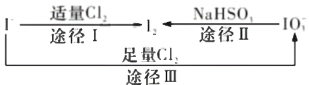
��Ŀ����
����Ŀ���л���1����3��5��7-����ϩ�������ƺϳ���ά��Ⱦ�ϡ�ҩ��ȣ���ṹ ��ʽΪ![]() �������ʵĺϳɷ�������ͼ��ʾ��
�������ʵĺϳɷ�������ͼ��ʾ��
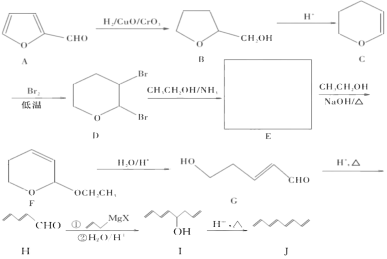
��1��1��3��5��7-����ϩ�ķ���ʽΪ______���л���A���������������� _______�������ƣ���
��2��E�Ľṹ��ʽΪ______.
��3��I��J�ķ�Ӧ����Ϊ______.
��4��![]() ��һ�������¿��Է����Ӿ۷�Ӧ���ϳ���֧������״�л��߷��ӡ�д���÷�Ӧ�Ļ�ѧ����ʽ: ________________________ .
��һ�������¿��Է����Ӿ۷�Ӧ���ϳ���֧������״�л��߷��ӡ�д���÷�Ӧ�Ļ�ѧ����ʽ: ________________________ .
��5������������G��ͬ���칹����___________�֡�
����̼��������Һ��Ӧ�������� �ڲ���ʹ��ˮ��ɫ
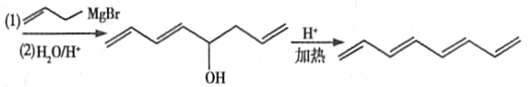
��6����CH3CHO �� HCHO��![]() Ϊԭ��Ҳ���Ժϳ�1��3��5��7-����ϩ����д���ϳ�·�ߡ��������Լ���ѡ��_____________________________________________________________________ .��֪��
Ϊԭ��Ҳ���Ժϳ�1��3��5��7-����ϩ����д���ϳ�·�ߡ��������Լ���ѡ��_____________________________________________________________________ .��֪��![]() ��
��
���𰸡�C8H10 ȩ����̼̼˫�����Ѽ� 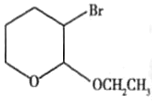 �ӳɷ�Ӧ
�ӳɷ�Ӧ ![]() 4 CH3CHO+HCHO
4 CH3CHO+HCHO![]()
![]()
![]()
![]()
��������
��1�����ݽṹ��ʽ������ͽڵ�Ϊ̼��������ļ���λ��ȫ��������ԭ�ӣ�1��3��5��7-����ϩ�ķ���ʽΪC8H10�������л���A�Ľṹ��ʽ������������������ȩ����̼̼˫�����Ѽ���
��Ϊ��C8H10��ȩ����̼̼˫�����Ѽ���
��2������ͼ�еĸ�����֮���ת����ϵ��֪��D��E���Ҵ��е�-OCH2CH3ȡ��D����O���ڵ�̼�ϵ���ԭ�ӣ�E��F����������ȥ��Ӧ��E����ȥ1��HBr ���ӣ��õ�F������E�Ľṹ��ʽΪ ��
��
����
��3����I��J�ķ�Ӧ��Ӧ�����У�I�е�һ��˫����Ϊ������������һ���ǻ���һ����ԭ��ת��ΪJ�������ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
��Ϊ���ӳɷ�Ӧ��
��4��![]() ��һ�������¿��Է����Ӿ۷�Ӧ���ϳ���֧������״�л��߷��ӡ�ԭ����˫��������ӣ������ļ��������Ϊ˫������ѧ����ʽΪ
��һ�������¿��Է����Ӿ۷�Ӧ���ϳ���֧������״�л��߷��ӡ�ԭ����˫��������ӣ������ļ��������Ϊ˫������ѧ����ʽΪ![]() ��
��
����![]()
��5��G�ķ���ʽΪC5 H8 O2��G��ͬ���칹����̼�����Ʒ�Ӧ���Բ������壬����ṹ�к���-COOH�����䲻��ʹ��ˮ��ɫ��������������ͬ���칹���� ��
��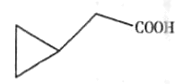 ��
��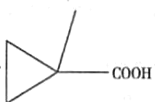 ��
��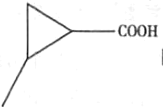 ������
������
����4��
��6��CH3CHO+HCHO![]()
![]()
![]()
![]()

����CH3CHO+HCHO![]()
![]()
![]()
![]()


����Ŀ����֪:�� X��Y��Z��W��R��QΪԭ��������������Ķ�����Ԫ�ء�X ������Ԫ����ԭ�Ӱ뾶��С��Ԫ�أ�Y���γɻ�������������Ԫ�أ�W�������������Ǵ�����������3����Q��Wͬ���壬Y��Rԭ�ӵ�����������֮�͵���Z��������������
������˹��������������1932�����electronegativity��ΪԪ��ԭ���ڻ�����ij�����ʵı�ȣ�electronegativity�Ĵ�С�����ж�Ԫ�ؽ�������ǽ�����ǿ�����±��г����ֶ�����Ԫ�ص�Electronegativity��ֵ��
Ԫ�� | X | Y | Z | W | R | Q |
electronegativity | 2.1 | 2.5 | 3.0 | 3.5 | 0.9 | 2.5 |
Ԫ�� | Mg | Li | Al | Cl | P | Be |
electronegativity | 1.2 | 1.0 | 1.5 | 3.0 | 2.1 | 1.5 |
��ش��������⣨�漰X��Y��Z��W��R��Qʱ����Ԫ�ط��ű�ʾ����
(1)�����ϱ����������ݣ���֪Ԫ�ص�electronegativityԽ��__(������ԡ��ǽ����ԡ�)Խǿ��
(2)Ԫ��Q�����ڱ��е�λ��Ϊ_________��
(3)W��R��Q���˼����Ӱ뾶�ɴ�С����˳��Ϊ______��
(4)Ԫ��X��Z��W֮�����γɶ���10����������д����Ӧ��Ͳ����ΪX��Z��W֮���γɵ�10��������һ�����ӷ���ʽ______________��
(5)һ����Ԫ��W��R��ɵİ�ɫ���廯��������ʽΪ_______________��
(6)�ԱȽ��ȶ��ԣ�X2W_____ X2Q���е㣺X2W_____ X2Q ���������������
(7)Ԫ�� X��Y��Z��W��R��Q�е�����Ԫ�ؿ��γ�ԭ�Ӹ�����Ϊ1��2�Ĺ��ۻ������������Ԫ�ص�ԭ������֮�������_________��
A��2 B��4 C��5 D��7