题目内容
9.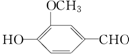 香兰素的结构简式如图所示,有宜人的芳香气味,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )
香兰素的结构简式如图所示,有宜人的芳香气味,是制作巧克力的辅助原料,下列关于香兰素的判断不正确的是( )| A. | 分子式为C8H8O3 | B. | 可与银氨溶液反应 | ||
| C. | 可与NaOH溶液反应 | D. | 分子中所有原子都在同一平面 |
分析 该物质中含有醚键、酚羟基和醛基、苯环,具有醚、酚、醛和苯的性质,能发生氧化反应、取代反应、加成反应、还原反应等,据此分析解答.
解答 解:A.根据结构简式知,分子式为C8H8O3,故A正确;
B.含有醛基,所以能发生银镜反应,故B正确;
C.含有酚羟基,具有酸性,所以能与NaOH溶液反应,故C正确;
D.含有甲基,所以所有原子不能可能位于同一平面上,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,把握官能团及其性质关系即可解答,侧重考查醛、酚的性质,难点是判断原子是否共面,易错选项是D.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
19.a、b、c、d、e、f、g为七种由短期周期元素构成的粒子,它们都有10个电子,其结构特点如下:
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可反应生成两个共价型g分子.
试写出:
(1)d分子的空间构型为三角锥形.
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:NaOH>Mg(OH)2 (用化学式表示).
(3)d溶于水的电离方程式NH3+H2O?NH3•H2O?NH4++OH-.
(4)g粒子所构成的晶体类型属分子晶体.
(5)c粒子是OH-,f粒子是H3O+(都用化学式表示).
| 粒子代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 单位电荷数 | 0 | 1+ | 1- | 0 | 2+ | 1+ | 0 |
试写出:
(1)d分子的空间构型为三角锥形.
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为:NaOH>Mg(OH)2 (用化学式表示).
(3)d溶于水的电离方程式NH3+H2O?NH3•H2O?NH4++OH-.
(4)g粒子所构成的晶体类型属分子晶体.
(5)c粒子是OH-,f粒子是H3O+(都用化学式表示).
20.下列措施或事实不能用勒夏特列原理解释的是( )
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | H2、I2、HI平衡混合气减小压强(扩大体积)可使颜色变浅 | |
| C. | 打开汽水瓶盖,有气泡冒出 | |
| D. | 在合成氨的反应中,加压有利于氨的合成 |
17.与CH2=CH2→CH2Br-CH2Br的变化属于同一反应类型的是( )
| A. | CH3COOH→CH3COOC2H5 | B. | C2H5Cl→CH2=CH2 | ||
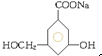
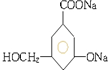
| C. | 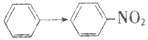 | D. | CH3CHO→C2H5OH |
1.下列各组物质中,反应后生成碱和氧气的是( )
| A. | 钾和水 | B. | 氧化钠和水 | C. | 氧化钙和水 | D. | 过氧化钠和水 |
18.完成下列各小题
(1)第34号元素符号是Se,铬元素位于元素周期表的d区(填“s、p、d、f、ds),其价层电子的轨道表示式(或电子排布图)为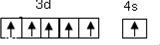
(2)用“>”或“<”填空
(3)在O、Na、P、Cl四种元素中,电负性最大的是O,PCl3的立体构型为三角锥形,中心原子的杂化轨道类型为sp3中心原子的价层电子对数为4
(4)在下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,共有4种(填数字)晶体类型,熔化时不需破坏化学键的是①⑤,(填序号,下同)熔化时只需破坏共价键的是④⑥.
(1)第34号元素符号是Se,铬元素位于元素周期表的d区(填“s、p、d、f、ds),其价层电子的轨道表示式(或电子排布图)为

(2)用“>”或“<”填空
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| P>S | O2->Na+ | CaO<MgO | HClO4>H2SO4 |
(4)在下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,共有4种(填数字)晶体类型,熔化时不需破坏化学键的是①⑤,(填序号,下同)熔化时只需破坏共价键的是④⑥.
 .
. .
.
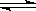 C(g)+2D(g);经5min达到平衡, 测得压强减小了10%,下列说法中正确的是
C(g)+2D(g);经5min达到平衡, 测得压强减小了10%,下列说法中正确的是