题目内容
【题目】实验室用如下图所示装置来制备乙炔,并验证乙炔的某些化学性质,制备的 乙炔气体中往往含有少量的 H2S 气体,请按下列要求填空:
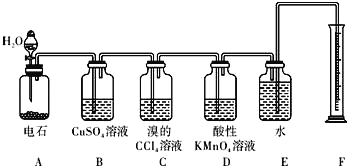
(1)实验室制乙炔的化学方程式是:_________________;为了得到较为平稳的乙炔气流, 装置 A 的分液漏斗中常用_____来代替水.
(2)装置 B 中CuSO4溶液的作用是_____.
(3)装置 D 中观察到的现象是_____
(4)若称取m g 电石,反应完全后,测得B处溴的CCl4溶液增重n g,则CaC2的纯度为_____(用m与n表示)。
【答案】 CaC2+2H2O﹣→CH≡CH↑+Ca(OH)2 饱和食盐水 除去 H2S 杂质,以防干扰后续实验 紫色或紫红色褪去 32n/13m
【解析】分析:实验室用电石和水反应制备乙炔,其中含有杂质,为了净化和检验乙炔气体,测定气体体积,则需要的装备依次为:气体制备装置、净化装置(除硫化氢)、检验装置、性质实验装置、排水测体积的装置,以此解答。
详解:(1)实验室制备乙炔是利用电石和水反应生成乙炔和氢氧化钙,反应的化学方程式为:CaC2+2H2O→CH≡CH↑+Ca(OH)2 ,碳化钙与水反应很剧烈,用饱和食盐水可以减缓反应,所以为了得到平稳的气流,用饱和食盐水代替水,
因此,本题正确答案是:CaC2+2H2O→CH≡CH↑+Ca(OH)2;饱和食盐水;
(2)硫化氢气体具有还原性,也会导致溴水、高锰酸钾溶液褪色,装置B中CuSO4溶液的作用是除去乙炔中的硫化氢,Cu2++H2S=CuS↓+2H+,防止干扰后续检验实验;
因此,本题正确答案是:除去 H2S 杂质,以防干扰后续实验;
(3)乙炔气体通过溴的四氯化碳溶液,会发生加成反应,装置C中观察到的现象是溶液褪色;
因此,本题正确答案是:紫色或紫红色褪去;
(4)若称取m g 电石,反应完全后,测得B处溴的CCl4溶液增重n g,则根据方程式:
C2H2+2Br2→CHBr2CHBr2可知乙炔的物质的量是![]() mol,所以CaC2的纯度为
mol,所以CaC2的纯度为![]() 100%=32n/13m。
100%=32n/13m。

 名校课堂系列答案
名校课堂系列答案