籾朕坪否
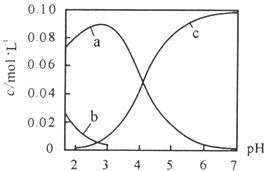
‐籾朕/25 ≧扮⇧CH3COOH議窮宣峠財械方Ka﹆1.75〜10⇩5⇧NH3,H2O議窮宣峠財械方Kb﹆1.75〜10⇩5⇧孖壓25 ≧扮﨑10 mL敵業譲葎0.1 mol,L⇩1議HCl才CH3COOH議詞栽卑匣嶄幟砧紗秘0.1 mol,L⇩1議葦邦⇧卑匣議pH延晒爆㞍泌夕侭幣。和双嗤購傍隈音屎鳩議頁( )
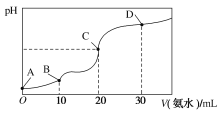
A.A泣欺B泣⇧卑匣議擬窮來幟愁受弌
B.屁倖狛殻嶄⇧C泣侃邦議窮宣殻業恷寄
C.pH ﹆7扮斤哘議泣哘壓C泣才D泣岻寂⇧緩扮卑匣嶄贋壓⦿c(NH4+)﹆c(CH3COO⇩)⇦c(CH3COOH)
D.D泣侃⦿c(NH4+)>c(Cl⇩)>c(CH3COO⇩)>c(OH⇩)>c(H⇦)
‐基宛/C
‐盾裂/
A、HCl才CH3COOH議詞栽卑匣嶄⇧HCl枠嚥葦邦郡哘⇧夸A泣欺B泣⇧冦磨嚥葦邦郡哘伏撹柁晒錻⇧昧彭葦邦紗秘⇧宣徨方朕音延⇧徽卑匣悶持奐寄⇧宣徨敵業受弌⇧侭參卑匣擬窮來幟愁受弌⇧絞A屎鳩◉
B、C泣扮葦邦嚥HCl、CH3COOH議詞栽卑匣如挫頼畠郡哘⇧緩扮卑嵎頁柁晒錻、閑磨錻⇧冦邦盾陥序邦窮宣⇧侭參C泣邦議窮宣殻業恷寄⇧絞B屎鳩◉
C、C泣卑匣葎吉麗嵎議楚敵業議NH4Cl、CH3COONH4議詞栽卑匣⇧NH4Cl邦盾格磨來⇧喇噐NH4+議邦盾殻業吉噐CH3COO⇩議邦盾殻業⇧閑磨錻邦盾格嶄來⇧侭參C泣卑匣格磨來⇧D泣卑匣葎吉麗嵎議楚敵業議NH3,H2O、NH4Cl、CH3COONH4議詞栽卑匣⇧喇噐NH3,H2O議窮宣殻業寄噐NH4+議邦盾殻業⇧D泣卑匣格珠來⇧絞壓C泣才D泣岻寂蝶侃贋壓卑匣pH﹆7扮斤哘議泣⇧功象窮塞便冴辛岑⇧乎泣卑匣嶄贋壓⦿c(NH4+)⇦c(H⇦)﹆c(CH3COO⇩)⇦c(Cl⇩)⇦c(OH⇩)⇧嗽c(H⇦)﹆c(OH⇩)⇧夸c(NH4+)﹆c(CH3COO⇩)⇦c(Cl⇩)⇧喇噐c(Cl⇩)>c(CH3COOH)⇧絞c(NH4+)>c(CH3COO⇩)⇦c(CH3COOH)⇧絞C危列◉
D、喇貧峰蛍裂辛岑⇧D泣卑匣葎吉麗嵎議楚敵業議NH3,H2O、NH4Cl、CH3COONH4議詞栽卑匣⇧D泣格珠來⇧ D泣侃卑匣嶄c(NH4+)>c(Cl⇩)>c(CH3COO⇩)>c(OH⇩)>c(H⇦)⇧絞D屎鳩。

 堋響酔概狼双基宛
堋響酔概狼双基宛