题目内容
已知A、B、C、D、E、F、G、H、I是中学化学中常见的九种化合物,其中B常温下为无色无味透明的液体,C焰色反应火焰呈黄色,E是红棕色的固体;X、Y是两种常见的单质,其中X常温常压下为气体。
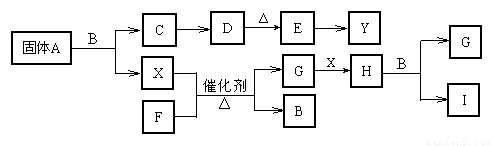
根据上面框图关系填空。
(1)A的化学式为________________,固体A的颜色为__________________;
(2)写出“X+F G+B”的化学反应方程式________________________;
G+B”的化学反应方程式________________________;
(3)写出“实验室中制取F气体”的化学反应方程式_____________________;
(4)写出“C→D”反应的离子方程式_________________________;
(5)写出“E+金属单质 Y+两性氧化物”的化学反应方程式___________________。
Y+两性氧化物”的化学反应方程式___________________。
练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
除去下列物质中的杂质选用的试剂和方法最合理的是( )
物质 | 杂质 | 试剂 | 方法 | |
A | 二氧化碳 | 二氧化硫 | NaOH溶液 | 洗气 |
B | 氯化亚铁溶液 | 氯化铁 | 过量铁粉 | 过滤 |
C | 氧化铁 | 氧化铝 | 氨水 | 过滤 |
D | 氯化钠溶液 | 碘化钠 | 四氯化 | 萃取 |
几种短周期元素的原子半径及主要化合价如下表:
元素代号 | L | M | X | R | T |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
下列叙述正确的是( )
A.离子半径大小:r(M3+)>r(T2-)
B.R的氧化物对应的水化物可能具有两性
C.X单质在氧气中燃烧生成XO3
D.L、X形成的简单离子核外电子数不相等


 碳
碳 )
)
 2CeT3(有机层)+6H+(水层)
2CeT3(有机层)+6H+(水层)