题目内容
下列各组性质的比较中正确的是( )
| A.酸性 HClO4<HBrO4<HIO4 | B.碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C.稳定性 HCl>PH3>H2S | D.还原性 Cl->Br->I- |
B
解析试题分析:A、Cl、Br、I非金属性依次减弱故最高价含氧酸酸性依次减弱,A错误;B、金属性Ba>Ca>Mg,故氢氧化物碱性依次减弱,正确;C、非金属性Cl>S>P,故氢化物稳定性HCl>H2S>PH3,C错误;D、非金属性Cl>Br>I,故还原性Cl-<Br-<I-,错误。答案为B。
考点:考查元素周期律的相关知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各分子中所有原子都满足最外层为8电子结构的是
| A.BeCl2 | B.PCl3 | C.PCl5 | D.H2S |
下列说法正确的是
| A.在周期表中金属和非金属的分界处寻找催化剂和耐高温、耐腐蚀的合金材料 |
| B.元素性质随着核电荷数的递增而呈周期性的变化叫元素周期律 |
| C.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| D.相对分子质量相同,而结构不同的化合物互称为同分异构体 |
随着科学技术的不断进步,研究物质的手段和途径越来越多,N5+、H3、O4、C60等已被发现。 下列有关说法中,正确的是
| A.N5+ 离子中含有36个电子 | B.H2与H3属于同素异形体 |
| C.C60的摩尔质量为720 | D.O2与O4属于同位素 |
根据表1信息,判断以下叙述正确的是( )
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
 A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<QC.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为:HXO4>H2YO4>H3ZO4,则下列判断中正确的是( )
| A.元素非金属性按X、Y、Z的顺序减弱 |
| B.原子的电子能力按X、Y、Z的顺序增强 |
| C.气态氢化物的稳定性按X、Y、Z的顺序增强 |
| D.单质的氧化性按X、Y、Z的顺序增强 |
Se是人体必需微量元素,下列有关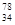 Se和
Se和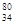 Se的说法正确的是( )
Se的说法正确的是( )
A.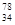 Se 和 Se 和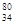 Se所含电子数不同 Se所含电子数不同 |
B.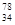 Se和 Se和 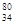 Se是两种不同的核素 Se是两种不同的核素 |
C.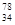 Se和 Se和 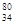 Se 分别含有44和46个质子 Se 分别含有44和46个质子 |
D.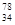 Se和 Se和 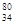 Se都含有34个中子 Se都含有34个中子 |
相对原子质量原来以16O原子质量的十六分之一为标准,以该标准得到的仍为整数的是
| A.14N的质量数 | B.碳原子的相对质量 |
| C.氯元素的相对原子质量 | D.氢氧化钠的摩尔质量 |
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是( )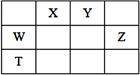
| A.X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B.由X、Y和氢三种元素形成的化合物中只有共价键 |
| C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 |
| D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |