题目内容
有30g由烧碱、小苏打及不与酸、碱反应也不溶于水的杂质组成的混合物,将其平均分为两等份做以下实验:(1)将第一份置于密闭容器中加热至250℃,充分反应后,将密闭容器中的气体导入过量澄清石灰水中,得到5g白色沉淀;(2)将第二份溶于水配成100mL溶液(除杂质外全部溶解),取10mL溶液能跟20mL 1mol/L的盐酸恰好中和.求混合物中杂质的质量分数.
答案:
解析:
解析:
|
解:对混合物加热发生的反应为:NaOH+NaHCO3=Na2CO3+H2O 1 ∶ 1 NaHCO3过量则:2NaHCO3 产生CO2说明NaHCO3过量 设混合物中NaOH的物质的量为x,NaHCO3的物质的量为y. (1) y-x=0.2 ① (2)NaOH+HCl=NaCl+H2O NaHCO3+HCl=NaCl+CO2↑+H2O 1 ∶ 1 1 ∶ 1 即n(HCl)=n(NaOH)+n(NaHCO3) x+y=0.02L×1mol/L×10×2 ② 解①、②式得:x=0.1mol,y=0.3mol. 杂质%= |

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
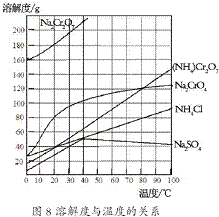 (2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下:
(2012?江苏一模)重铬酸铵[(NH4)2Cr2O7]是一种桔黄色结晶,可用作有机合成催化剂、实验室制纯净的N2及Cr2O3等.实验室可由工业级铬酸钠(Na2CrO4)为原料制取.有关物质溶解度如图所示.实验步骤如下: