题目内容
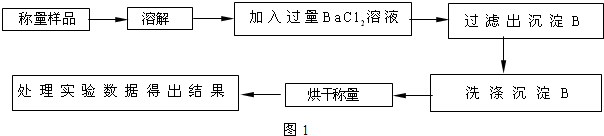
8. 流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定.北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O.下列说法不正确的是( )
流动电池是一种新型电池.其主要特点是可以通过电解质溶液的循环流动,在电池外部调节电解质溶液,以保持电池内部电极周围溶液浓度的稳定.北京化工大学新开发的一种流动电池如图所示,电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O.下列说法不正确的是( )| A. | a为负极,b为正极 | |
| B. | 该电池工作时PbO2电极附近溶液的pH增大 | |
| C. | a极的电极反应为Cu-2e-═Cu2+ | |
| D. | 调节电解质溶液的方法是补充CuSO4 |
分析 根据电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,则铜失电子发生氧化反应为负极,反应式为:Cu-2e-═Cu2+,PbO2得电子发生还原反应为正极,反应式为:PbO2+4H++SO42-+2e-═PbSO4+2H2O,据此分析.
解答 解:A.根据电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,则铜失电子发生氧化反应为负极,PbO2得电子发生还原反应为正极,所以为负极,b为正极,故A正确;
B.PbO2得电子发生还原反应为正极,反应式为:PbO2+4H++SO42-+2e-═PbSO4+2H2O,所以PbO2电极附近溶液的pH增大,故B正确;
C.铜失电子发生氧化反应为负极,反应式为:Cu-2e-═Cu2+,故C正确;
D.由电池总反应为Cu+PbO2+2H2SO4═CuSO4+PbSO4+2H2O,则调节电解质溶液的方法是补充H2SO4,故D错误;
故选D.
点评 本题考查了化学电源新型电池,根据原电池原理来分析解答,知道电极上发生的反应即可解答,电极反应式的书写是学习难点,总结归纳书写规律,难度中等.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
4.金属的下列性质中,与金属的晶体结构无关的是( )
| A. | 易导电 | B. | 易导热 | C. | 有延展性 | D. | 易锈蚀 |
5. 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
①向溶液中加入1~2滴指示剂.
②取20.00mL标准溶液放入锥形瓶中.
③用氢氧化钠溶液滴定至终点.
④重复以上操作.
⑤配制250mL盐酸标准溶液.
⑥根据实验数据计算氢氧化钠的物质的量浓度.
(1)以上各步中,正确的操作顺序是⑤②①③④⑥(填序号),上述②中使用的仪器除锥形瓶外,还需要酸式滴定管,使用酚酞作指示剂.
(2)滴定并记录V(NaOH)的初、终读数.数据记录如下表:
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积为
V(NaOH)=$\frac{19.98+20.00+20.80+20.02}{4}$mL=20.02mL
他的计算合理吗?不合理.理由是第3组数据明显偏大,不应采用.
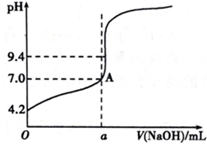
通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如下图所示,则a< 20.02(填“>”“<”或“=”).
 现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:
现用盐酸标准溶液来测定NaOH溶液的浓度.滴定时有下列操作:①向溶液中加入1~2滴指示剂.
②取20.00mL标准溶液放入锥形瓶中.
③用氢氧化钠溶液滴定至终点.
④重复以上操作.
⑤配制250mL盐酸标准溶液.
⑥根据实验数据计算氢氧化钠的物质的量浓度.
(1)以上各步中,正确的操作顺序是⑤②①③④⑥(填序号),上述②中使用的仪器除锥形瓶外,还需要酸式滴定管,使用酚酞作指示剂.
(2)滴定并记录V(NaOH)的初、终读数.数据记录如下表:
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(标准溶液)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
V(NaOH)=$\frac{19.98+20.00+20.80+20.02}{4}$mL=20.02mL
他的计算合理吗?不合理.理由是第3组数据明显偏大,不应采用.
通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如下图所示,则a< 20.02(填“>”“<”或“=”).
2.下列关于常见有机化合物说法正确的是( )
| A. | 甲烷、乙烯和苯都可以从化石燃料中提取,都能使溴水因发生化学反应而褪色 | |
| B. | 乙烯和苯分子中因都存在C═C,因为都能发生加成反应和氧化反应 | |
| C. | 酸性KMnO4溶液既可鉴别乙烷与乙烯,又可除去乙烷中的乙烯而得到纯净的乙烷 | |
| D. | 只用一种试剂就可以鉴别乙醇、乙酸、四氯化碳、苯四种液体 |
13.据国外资料报道,在一种共生矿--独居石中,查明有尚未命名的116号元素,判断116号元素应位于周期表中的( )
| A. | 第6周期ⅣA族 | B. | 第7周期Ⅶ族 | C. | 第7周期ⅥA族 | D. | 第8周期ⅥA族 |
17.下列说法正确的是( )
| A. | 化学反应都是吸热反应 | |
| B. | 化学反应都是放热反应 | |
| C. | 物质发生化学反应都伴随着能量变化 | |
| D. | 有能量变化的物质变化都是化学变化 |
 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.