题目内容
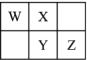
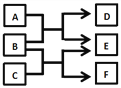
【题目】中学常见无机物A、B、C、D、E、X均由短周期元素组成,且存在如图转化关系(部分反应物、生成物和反应条件略去).下列推断不正确的是( ) 
A.若X是Na2SO3 , C是能使品红溶液褪色的气体,则A可能是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH﹣+HCO3﹣═H2O+CO32﹣ 则E﹣定能还原CuO
C.若B,X均为单质,D为CO,C能和E反应,则E为NaOH
D.若D为白色沉淀,且与A的摩尔质量相等,则X一定是铝盐
【答案】A
【解析】解:A.若X是Na2SO3 , 则A可能是氯气,则B为HCl,E为HClO,C为气体SO2 , D为NaHSO3 , D和E能发生氧化还原反应,与题干说法不相符,故A错误; B.根据B、D反应的离子方程式OH﹣+HCO3﹣═H2O+CO32﹣ , A为活泼金属Na,B为NaOH、E为H2 , X为CO2 , C为Na2CO3 , D为NaHCO3 , H2在加热时能还原Fe2O3 , 故B正确;
C.若B、X均为单质,D为CO,C能和E反应,则C为CO2 , B为氧气,C为碳单质,A为过氧化钠,过氧化钠与水反应生成ENaOH和氧气,符号条件,故C正确;
D.D为摩尔质量为78g/mol的Al(OH)3 , A为摩尔质量为78g/mol 的Na2O2 , X为铝盐,C为偏铝酸盐,铝盐和偏铝酸盐在溶液中发生双水解反应生成Al(OH)3 , 符合转化关系,故D正确;
故选A.
A.若X是Na2SO3 , 则A可能是氯气,则B为HCl,E为HClO,C为气体SO2 , D为NaHSO3 , D和E能发生氧化还原反应;
B.根据B、D反应的离子方程式OH﹣+HCO3﹣═H2O+CO32﹣ , A为活泼金属Na,B为NaOH、E为H2 , X为CO2 , C为Na2CO3 , D为NaHCO3;
C.若B、X均为单质,D为CO,C能和E反应,则C为二氧化碳,B为氧气,A为过氧化钠,E为NaOH;
D.D为白色沉淀,可以判断为OH﹣与Al 铝离子生成偏铝酸根,偏铝酸根离子再与铝离子生成Al(OH)3 , X为铝盐,C为偏铝酸盐,铝盐和偏铝酸盐在溶液中发生双水解反应生成Al(OH)3 .

 华东师大版一课一练系列答案
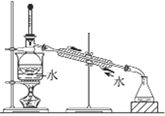
华东师大版一课一练系列答案【题目】利用下列装置和操作不能达到实验目的的是( )
|
|
|
|
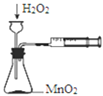
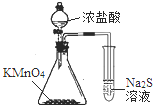
A.从含碘CCl4溶液中提取碘和回收CCl4溶剂 | B.萃取操作过程中的放气 | C.定量测定化学反应速率 | D.比较KMnO4、Cl2、S的氧化性 |
A. A B. B C. C D. D