��Ŀ����
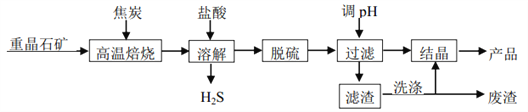
����Ŀ����ˮ�Ȼ������壨BaCl22H2O���ڹ�ҵ����Ҫ����������ֱ��Ρ����Ϻ��л�Ⱦ�ϣ�ij�о�С�����ؾ�ʯ����Ҫ�ɷ� BaSO4���Ʊ�BaCl22H2O ��������ͼ��
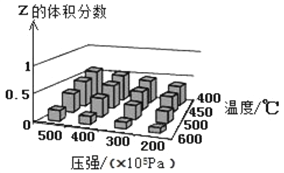
��1����֪��
�� BaSO4(s)+ 4C(s)= 4CO(g) + BaS(s) ��H1 = 571.2kJmol��1
�� C(s)+ CO2(g)= 2CO(g) ��H2 = 172.5 kJmol��1
��Ӧ BaSO4(s)+ 2C(s)= 2CO2(g)+ BaS(s)����H = _____ kJmol��1
��2�����±�������������̿��ͬʱ��Ҫͨ���������Ŀ����_____��_____��
��3����������з�Ϊ������ ��һ������������ �ڶ����ǻ�ѧ����
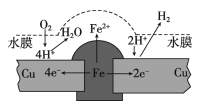
�� ����������ֱ�����������£����ÿ���������������ȥ��������_____��
�� �������ʲ����������������_____ (����ĸ)��
A. ������� B. �������� C. ˫��ˮ D.����
��4������������ϴ����������ҪĿ����_____��
��5���ܽ�ʱ������ H2S ���� 80~85 ��ʱ��ʯ�ҵ��Ͻ�(CaCN2�Ľ�ˮ�����)���ղ��Ƶø��м�ֵ�IJ�Ʒ��������[CS(NH2)2]����ʯ�ҡ���д���Ʊ�����Ļ�ѧ����ʽ_____��
���𰸡� 226.2 ʹ BaSO4�õ���ֵĻ�ԭ������� BaS�IJ����� �٢�Ϊ���ȷ�Ӧ��̿��������Ӧ����ά�ַ�Ӧ������� H2S AB ���ٷ����п����Ա��ζԻ�������Ⱦ���������𰸾��ɣ� H2S + CaCN2+ 2H2O = CS(NH2)2+Ca(OH)2
����������1���ɸ�˹���������H=��H1��2����H2= 226.2��
��2�����±�������������̿��ͬʱ��Ҫͨ���������Ŀ����ʹ BaSO4�õ���ֵĻ�ԭ���൱�ڽ������ã�������� BaS�IJ�������ͬʱ��Ӧ�٢�Ϊ���ȷ�Ӧ��̿��������Ӧ����ά�ַ�Ӧ������£���3��������������ֱ�����������£�������������Һ�е��ܽ�ȣ��ÿ���������������H2S�������Һ�С�����������ȥ�������������ܽ����Һ�д��ڴ��������ӣ��ø�����ء����������������ʱ��H2S�������Ӿ���֮��Ӧ��������ء��������Ƶ���������ͬʱ�����ܻ������Ⱦ���������壬�ʲ���AB����4�����������ؽ������ӣ��Ի�����Ӱ�죬ϴ����������ҪĿ���Ǽ��ٷ����п����Ա��ζԻ�������Ⱦ����5��������������Ӧ��������д���Ʊ�����Ļ�ѧ����ʽ��H2S + CaCN2+ 2H2O = CS(NH2)2+Ca(OH)2��

 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�