题目内容
阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定错误的是
- A.12.5 mL 16 mol/L浓硫酸与足量铜共热,可生成SO2的分子数约为6.02×1022
- B.2.3 g 钠与O2完全反应时,转移电子数约为6.02×1022
- C.非标准状况下1.7gNH3体积为2.24 L
- D.16.9 g 过氧化钡(BaO2)固体中阴、阳离子总数约为0.2×6.02×1023
A
分析:A、浓硫酸和过量铜反应,随反应进行浓度变稀后不能与铜反应;
B、质量换算物质的量结合钠最外层电子数为1,分析;
C、非标准状况下0.1mol氨气可能为2.24L;
D、质量换算物质的量,结合过氧化钡是钡离子和过氧根离子构成分析;
解答:A、浓硫酸和过量铜反应,随反应进行浓度变稀后不能与铜反应;12.5 mL 16 mol/L浓硫酸中溶质物质的量0.2mol,与足量铜共热,生成SO2的分子数小于6.02×1022,故A错误;
B、2.3 g 钠物质的量为0.1mol,与O2完全反应时,转移电子数约为6.02×1022,故B正确;
C、非标准状况下1.7gNH3物质的量0.1mol,一定条件下体积可以为2.24 L,故C正确;
D、16.9 g 过氧化钡(BaO2)物质的量=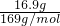 =0.1mol,固体中阴、阳离子是钡离子和过氧根离子,总数约为0.2×6.02×1023,故D正确;
=0.1mol,固体中阴、阳离子是钡离子和过氧根离子,总数约为0.2×6.02×1023,故D正确;
故选A.
点评:本题考查了阿伏伽德罗常数的应用,主要考查浓硫酸性质应用,质量换算物质的量计算微粒数,稀硫酸不能和铜反应,过氧化钡是钡离子和过氧根离子构成是解题关键,题目难度中等.
分析:A、浓硫酸和过量铜反应,随反应进行浓度变稀后不能与铜反应;
B、质量换算物质的量结合钠最外层电子数为1,分析;
C、非标准状况下0.1mol氨气可能为2.24L;
D、质量换算物质的量,结合过氧化钡是钡离子和过氧根离子构成分析;
解答:A、浓硫酸和过量铜反应,随反应进行浓度变稀后不能与铜反应;12.5 mL 16 mol/L浓硫酸中溶质物质的量0.2mol,与足量铜共热,生成SO2的分子数小于6.02×1022,故A错误;
B、2.3 g 钠物质的量为0.1mol,与O2完全反应时,转移电子数约为6.02×1022,故B正确;
C、非标准状况下1.7gNH3物质的量0.1mol,一定条件下体积可以为2.24 L,故C正确;
D、16.9 g 过氧化钡(BaO2)物质的量=
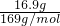 =0.1mol,固体中阴、阳离子是钡离子和过氧根离子,总数约为0.2×6.02×1023,故D正确;
=0.1mol,固体中阴、阳离子是钡离子和过氧根离子,总数约为0.2×6.02×1023,故D正确;故选A.
点评:本题考查了阿伏伽德罗常数的应用,主要考查浓硫酸性质应用,质量换算物质的量计算微粒数,稀硫酸不能和铜反应,过氧化钡是钡离子和过氧根离子构成是解题关键,题目难度中等.

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A、4 g重水(D2O)中所含质子数为0.2×6.02×1023 | B、2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2×6.02×1023 | C、4.48 L H2和O2的混合气体中所含分子数为0.2×6.02×1023 | D、0.2 mol Cl2溶解于等体积的水中,转移电子数为0.2×6.02×1023 |
 阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )
阿伏加德罗常数约为6.02×1023mol-1,下列说法中一定正确的是( )