题目内容
【题目】如图为浓硫酸与铜反应及其产物检验的实验装置,回答下列问题:
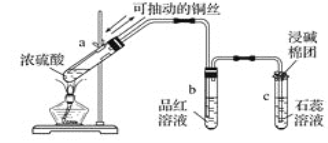
(1)指出试管a、b、c中产生的实验现象:
①a中__________________________;
②b中__________________________;
③c中__________________________。
(2)写出浓硫酸与铜反应的化学方程式:_____________。
【答案】铜丝溶解,有气泡生成 品红溶液褪色 石蕊溶液变红 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
【解析】
本题考查的是浓硫酸的性质、二氧化硫的性质。
铜与浓硫酸在加热条件下反应生成二氧化硫、硫酸铜和水。实验现象是铜丝溶解,有气泡生成。实验产生的二氧化硫具有漂白性,能使品红褪色,二氧化硫为酸性气体,能使石蕊溶液变红。据此解答。
(1)铜与浓硫酸在加热条件下反应生成二氧化硫、硫酸铜和水,方程式:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
①a中的现象为铜丝溶解,有气泡生成。本小题答案为:铜丝溶解,有气泡生成。
②a中产生的气体为SO2,SO2具有漂白性能使品红褪色,则b中的现象为品红褪色。本小题答案为:品红溶液褪色。
③a中产生的气体为SO2,SO2与石蕊溶液中的水反应生成H2SO3,石蕊溶液遇酸变红,c中的现象为石蕊溶液变红。本小题答案为:石蕊溶液变红。
(2)根据(1)中分析,铜与浓硫酸在加热条件下反应生成二氧化硫、硫酸铜和水,方程式:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。本小题答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O。本小题答案为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。

【题目】实验室制取氯气除了用浓盐酸和二氧化锰反应外还可利用下列反应:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O,该反应的优点是反应产生氯气速度快、不需加热.图是实验室利用此反应制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)上述反应中氧化剂和还原剂物质的量之比是______ ,若反应中氧化产物比还原产物多 1mol,则转移的电子数目为______ 。
(2)装置B的作用是______ ,实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象:_________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入______ (选“a”“b”或“c”)
a | b | c | |
Ⅰ | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E 的目的是为了比较Cl2、Br2、I2的氧化性强弱.已知Br2的水溶液因浓度不同而呈现橙色或红棕色,I2难溶于水而易溶苯,且I2的苯溶液为紫红色.当向D中缓缓通入足量Cl2时,可以看到无色溶液逐渐变为红棕色,说明Cl2的氧化性大于Br2,请写出D中对应的离子方程式并用单线桥法表示出电子转移情况:__________________ .打开活塞,将 D中的少量溶液加入E中,振荡E,观察到E中溶液分为两层,上层(苯层)为紫红色.该现象______ (填“能”或“不能”)说明 Br2的氧化性大于I2。
(5)装置F的作用是除去污染性的物质(Cl2、Br2等),已知 Cl2与NaOH反应时产物中可能有NaCl、NaClO、NaClO3,且![]() 值与温度高低有关.若烧杯中装有 500mL0.2mol/L 的NaOH溶液,则最多可吸收标况下的Cl2的体积为______ L(忽略Cl2溶于水)。
值与温度高低有关.若烧杯中装有 500mL0.2mol/L 的NaOH溶液,则最多可吸收标况下的Cl2的体积为______ L(忽略Cl2溶于水)。