题目内容
(1)氯酸钾熔化,粒子间克服了
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有
(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:A.
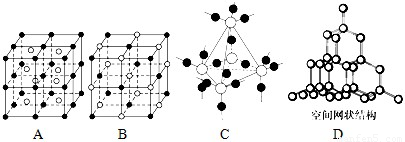
(5)图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称: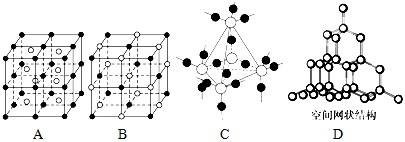
A.
离子键
离子键
的作用力;二氧化硅熔化,粒子间克服了共价键
共价键
的作用力;碘的升华,粒子间克服了分子间
分子间
的作用力.三种晶体的熔点由高到低的顺序是SiO2>KClO3>I2
SiO2>KClO3>I2
.(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为
①⑤③②④⑥
①⑤③②④⑥
(填序号).(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有
CO2
CO2
,由非极性键形成的非极性分子有H2
H2
,能形成分子晶体的物质是H2、CO2、HF
H2、CO2、HF
,含有氢键的晶体的化学式是HF
HF
,属于离子晶体的是(NH4)2SO4
(NH4)2SO4
,属于原子晶体的是SiC
SiC
,五种物质的熔点由高到低的顺序是SiC>(NH4)2SO4>HF>CO2>H2
SiC>(NH4)2SO4>HF>CO2>H2
.(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:A.
金属晶体
金属晶体
;B.分子晶体
分子晶体
;C.离子晶体
离子晶体
;D.原子晶体
原子晶体
.(5)图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:

A.
CsCl
CsCl
;B.NaCl
NaCl
;C.SiO2
SiO2
;D.金刚石
金刚石
.分析:(1)氯酸钾是离子晶体熔化时破坏离子键,二氧化硅是原子晶体熔化时破坏共价键,碘是分子晶体,升华时粒子间克服分子间作用力;熔点:原子晶体>离子晶体>分子晶体;
(2)根基晶体类型分析,原子晶体>离子晶体>分子晶体;
(3)根据组成元素及微粒之间的化学键分析;
(4)根据晶体的物理性质分析;
(5)根据晶体结构模型判断物质的种类;
(2)根基晶体类型分析,原子晶体>离子晶体>分子晶体;
(3)根据组成元素及微粒之间的化学键分析;
(4)根据晶体的物理性质分析;
(5)根据晶体结构模型判断物质的种类;
解答:解:(1)氯酸钾是离子晶体熔化时破坏离子键,二氧化硅是原子晶体熔化时破坏共价键,碘是分子晶体,升华时粒子间克服分子间作用力;熔点:原子晶体>离子晶体>分子晶体,所以熔点大小顺序为:SiO2>KClO3>I2;故答案为:离子键 共价键 分子间 SiO2>KClO3>I2;
(2)根基晶体类型分析,原子晶体>离子晶体>分子晶体,Si和金刚石都是原子晶体,原子半径越小,共价键越强,熔点越高,CO2和CS2都是分子晶体,相对分子质量越大熔点越高,所以熔点低到高的顺序为:①⑤③②④⑥;故答案为:①⑤③②④⑥;
(3)由极性键形成的非极性分子有CO2,由非极性键形成的非极性分子有H2,能形成分子晶体的物质是 H2、CO2、HF,含有氢键的晶体的化学式是 HF,属于离子晶体的是(NH4)2SO4,属于原子晶体的是SiC,五种物质的熔点由高到低的顺序是 SiC>(NH4)2SO4>HF>CO2>H2,故答案为:CO2 H2 H2、CO2、HF HF (NH4)2SO4 SiC SiC>(NH4)2SO4>HF>CO2>H2;
(4)根据晶体的物理性质分析,
A.固态时能导电,能溶于盐酸,属于金属晶体;
B.能溶于CS2,不溶于水,属于分子晶体;
C.固态时不导电,液态时能导电,可溶于水,属于离子晶体;
D.固态、液态时均不导电,熔点为3 500℃,属于原子晶体;
故答案为:金属晶体 分子晶体 离子晶体 原子晶体;
(5)由晶胞结构模型可知A、B、C、D分别为氯化铯、氯化钠、二氧化硅、金刚石,
故答案为:氯化铯;氯化钠;二氧化硅;金刚石;
(2)根基晶体类型分析,原子晶体>离子晶体>分子晶体,Si和金刚石都是原子晶体,原子半径越小,共价键越强,熔点越高,CO2和CS2都是分子晶体,相对分子质量越大熔点越高,所以熔点低到高的顺序为:①⑤③②④⑥;故答案为:①⑤③②④⑥;
(3)由极性键形成的非极性分子有CO2,由非极性键形成的非极性分子有H2,能形成分子晶体的物质是 H2、CO2、HF,含有氢键的晶体的化学式是 HF,属于离子晶体的是(NH4)2SO4,属于原子晶体的是SiC,五种物质的熔点由高到低的顺序是 SiC>(NH4)2SO4>HF>CO2>H2,故答案为:CO2 H2 H2、CO2、HF HF (NH4)2SO4 SiC SiC>(NH4)2SO4>HF>CO2>H2;
(4)根据晶体的物理性质分析,
A.固态时能导电,能溶于盐酸,属于金属晶体;
B.能溶于CS2,不溶于水,属于分子晶体;
C.固态时不导电,液态时能导电,可溶于水,属于离子晶体;
D.固态、液态时均不导电,熔点为3 500℃,属于原子晶体;
故答案为:金属晶体 分子晶体 离子晶体 原子晶体;
(5)由晶胞结构模型可知A、B、C、D分别为氯化铯、氯化钠、二氧化硅、金刚石,
故答案为:氯化铯;氯化钠;二氧化硅;金刚石;
点评:本题考查了晶体的有关性质,侧重考查学生分析问题、解决问题的能力.也有了培养学生的逻辑思维能力和抽象思维能力,也有助于调动学生的学习兴趣和学习积极性,提高学生的学习效率.

练习册系列答案
相关题目