题目内容
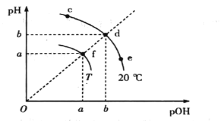
【题目】已知:2M(g)![]() N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )
N(g);△H <0。现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如右图所示。下列说法正确的是( )

A.a、b、c、d四个点中处于平衡状态的点是a、b、d
B.反应进行至25min时,曲线发生变化的原因是加入了 0.4molN
C.若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度
D.若40min后出现如图所示变化,则可能是加入了某种催化剂
【答案】C
【解析】
A. 根据图象可知在a、b、c、d四个点中处于平衡状态的点是物质的量浓度不变的状态,是b、d,A错误;
B. 由于反应物是M,生成物是N,在反应开始进行时不知道反应是正向进行还是逆向进行,所以至25min时,其中一种物质的浓度没变,而另一种物质的浓度突然增大,所以不能确定是反应物还是生成物增加,B错误;
C. 在35min时物质N平衡浓度大于15min时的,所以根据温度对化学平衡移动的影响,应该使平衡逆向移动,由于正反应是放热的,所以若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度,C正确;
D. 若40min后出现如图所示变化,即物质的浓度增大,但是都不再发生变化,说明平衡没有发生移动,则不可能是加入了某种催化剂,D错误;
答案选C。

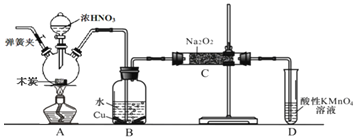
【题目】某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:

请你帮助该同学整理并完成实验报告:
(1)实验目的:_______________。
(2)实验用品:
仪器:________________;药品:__________。
(3)实验内容:(填写题给信息表中的序号)_____
实验方案 | 实验现象 | 有关化学方程式 |
_____ | _____ | _____ |
_____ | _____ | _____ |
_____ | _____ | _____ |
_____ | _____ | _____ |
_____ | _____ | _____ |
_____ | _____ | _____ |
(4)实验结论:____________。
(5)请用物质结构理论简单说明具有上述结论的原因。__________
(6)请你补充两组简单易行的实验方案,证明此周期中另外两种元素的性质递变规律。_________