题目内容
11.CO(g)与H2O(g)反应过程的能量变化如图所示,有关两者反应说法正确的是( )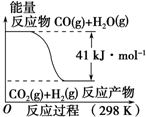
| A. | 该反应为吸热反应 | |
| B. | 1molCO(g)和1mol H2O(g)所具有的总能量大于1molCO2(g)和1molH2(g)具有的总能量 | |
| C. | 反应的热化学方程式:CO(g)+H2O(g)═CO2(g)+H2(g);△H=+41kJ•mol-1 | |
| D. | 1molCO2(g)和1molH2(g)反应生成1molCO(g)和H2O(g)要放出41kJ的热量 |
分析 A、考虑反应物和生成物的能量相对大小与反应的吸放热之间的关系;
B、根据反应热和物质具有能量的关系来回答判断;
C、由图可知,反应为放热反应;
D、考虑正反应反应热和逆反应反应热的关系
解答 解:A、从图示可知,反应物能量高生成物能量低,所以该反应为放热反应,故A错误;
B、从图示可知,反应物的能量高,生成物能量低,CO(g)与H2O(g)所具有的总能量大于 CO2(g)与H2(g)所具有的总能量,故B正确;
C、从图示可知,正反应为放热反应,正确的热化学方程式为:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ/mol,故C错误;
D、从图示可知,正反应为放热反应,则逆反应为吸热反应,所以1molCO2(g)和1molH2(g)反应生成1molCO(g)和H2O(g)要吸收41kJ的热量,故D错误;
故选:B.
点评 本题考查化学反应中的能量变化与图象分析,明确反应热的表示方法、热化学反应方程式的书写即可解答,要明确正逆反应的反应热大小相等,符号相反.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.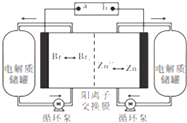 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环,下列说法正确的是( )| A. | 充电时电极a连接电源的负极 | |
| B. | 放电时负极的电极反应式为2Br--2e-═Br2 | |
| C. | 放电时左侧电解质储罐中的离子总浓度增大 | |
| D. | 充电时右侧电极变粗.电解质溶液浓度減小 |
2.微型银锌电池钮扣电池有广泛应用,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:
Zn+2OH--2e-═ZnO+H2O;Ag2O+H2O+2e-═2Ag+2OH-,根据上述反应式,判断下列叙述中正确的是( )
Zn+2OH--2e-═ZnO+H2O;Ag2O+H2O+2e-═2Ag+2OH-,根据上述反应式,判断下列叙述中正确的是( )
| A. | 在使用过程中,电池负极区溶液的碱性增强 | |
| B. | 使用过程中,电子由Ag2O极经外电路流向Zn极 | |
| C. | Zn是负极,Ag2O是正极 | |
| D. | Zn电极发生还原反应,Ag2O电极发生氧化反应 |
3.下列说法正确的是( )
| A. | 因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊试液褪色 | |
| B. | 能使品红溶液褪色的气体不一定是SO2 | |
| C. | SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色,其原理相同 | |
| D. | 将SO2与Cl2混合后通入品红溶液中漂白效果更好 |