题目内容
在T℃时,将ag NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为W,其中含NH4+的物质的量为bmol。下列叙述中正确的是 ( )
A.溶质的质量分数为 |
| B.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w |
C.溶液中 |
D.溶质的物质的量浓度 |
D
解析试题分析:A、氨水溶液溶质为氨气,该溶液的密度为ρ g?cm-3,体积为VmL,所以溶液质量为ρVg,溶质氨气的质量为ag,溶质的质量分数为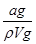 ×100%,故A错误;B、水的密度比氨水的密度大,相等体积的氨水与水,水的质量大,等体积混合后溶液的质量大于原氨水的2倍,溶液中氨气的质量相同,等体积混合所得溶液溶质的质量分数小于0.5w,故B错误;C、溶液OH-中来源于一水合氨、水的电离,NH4+的浓度为
×100%,故A错误;B、水的密度比氨水的密度大,相等体积的氨水与水,水的质量大,等体积混合后溶液的质量大于原氨水的2倍,溶液中氨气的质量相同,等体积混合所得溶液溶质的质量分数小于0.5w,故B错误;C、溶液OH-中来源于一水合氨、水的电离,NH4+的浓度为 =
=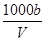 mol/L,一水合氨电离NH3?H2O
mol/L,一水合氨电离NH3?H2O NH4++OH-,一水合氨电离出的OH-为
NH4++OH-,一水合氨电离出的OH-为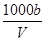 mol/L,所以溶液中OH-浓度大于
mol/L,所以溶液中OH-浓度大于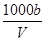 mol/LL,故C错误;D、a g NH3的物质的量为
mol/LL,故C错误;D、a g NH3的物质的量为 mol,溶液体积为VmL,所以溶液的物质的量浓度为
mol,溶液体积为VmL,所以溶液的物质的量浓度为 mol/L,故D正确,答案选D。
mol/L,故D正确,答案选D。
考点:考查物质的量浓度、质量分数的计算与相互关系等

 53天天练系列答案
53天天练系列答案
| |||||||||||||||
500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液恰好反应完全;另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
| A.(l0b - 5a) mol/L | B.( )mol/L )mol/L | C.(5b一 )mol/L )mol/L | D.(2b—a)mol/L |
设NA为阿伏加德罗常数,下列叙述中正确的是 ( )
| A.标准状况下,2.24 L苯中约含有个NA碳原子 |
| B.标准状况下,22.4 L H2中含中子数为2NA |
| C.1 L 1 mol/L醋酸溶液中离子总数为2 NA |
| D.1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2 NA个电子 |
下列化学用语正确的是 ( )
A.CH3COOH的球棍模型 |
B.第三周期简单阴离子结构示意图均可表示为 |
| C.HIO结构式为 H-I-O |
| D. 37Cl 中的37代表该原子的相对原子质量 |
a升CO和O2的混和气体,点燃后得到b升气体(前后条件相同),则混和气体中CO的体积可能是下列组合中的 ( )
①b ②2a/3 ③a-b ④a+b ⑤2(a-b)
| A.①②③ | B.②④⑤ | C.①②④ | D.①②⑤ |
下图是某盐酸试剂标签部分内容,据此判断
| A.该盐酸与钠可存放在同一药品橱柜中 |
| B.该盐酸含HCI质量为600 g |
| C.配制1OO mLO.2 mol/L盐酸需用到玻璃仪器为量筒、烧杯、玻璃棒 |
| D.该盐酸的物质的量浓度为12. 0 mol/L |
NA代表阿伏加德罗常数的值,下列有关叙述正确的是
| A.1mol乙烷(CH3CH3)中含有共价键的数目为6NA |
| B.由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA |
| C.标准状况下,22.4LH2O中含氢原子数为2NA |
| D.制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA |