题目内容
17.混合物分离的方法在生产、生活和科学实验中有着广泛的应用.请指出下列做法中,分别应用了哪种分离方法?(1)除去水中的泥沙过滤
(2)从溴水中提取溴萃取
(3)用海水晒盐蒸发
(4)海水淡化蒸馏.
分析 (1)泥沙不溶于水;
(2)溴不易溶于水,易溶于有机溶剂;
(3)晒盐时水挥发;
(4)海水中水的沸点低.
解答 解:(1)泥沙不溶于水,则选择过滤法分离,故答案为:过滤;
(2)溴不易溶于水,易溶于有机溶剂,则选择有机溶剂萃取分离,故答案为:萃取;
(3)晒盐时水挥发,则海水晒盐为蒸发原理,故答案为:蒸发;
(4)海水中水的沸点低,则利用蒸馏法海水淡化,故答案为:蒸馏.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.用括号内的试剂除去下列各物质中少量的杂质,正确的是( )
| A. | 溴苯中的溴(碘化钾溶液) | B. | 硝基苯中的硝酸(氢氧化钠溶液) | ||
| C. | 乙烷中的乙烯(氢气) | D. | 苯中的甲苯(水) |
5.下列检验试样中某离子的操作及结论不合理的是( )
| A. | 先加HCl无明显现象,再加BaCl2有白色沉淀,一定有SO42- | |
| B. | 加入稀盐酸产生能使澄清石灰水变浑浊的无味气体,则溶液中一定有CO32- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 做焰色反应,末观察到焰色为紫色,则待测液中一定不含有钾元素 |
12.下列现象不能用氢键解释的是( )
| A. | 冰的密度小于液态水 | B. | NH3容易液化 | ||
| C. | NH3极易溶于水 | D. | HF分子比HCl分子稳定 |
2.建设资源节约型、环境友好型社会是政府的工作目标,以下措施中不能体现这一思想的是( )
| A. | 在电解铝工业中添加冰晶石 | |
| B. | 开发太阳能、风能、氢能等清洁能源 | |
| C. | 收集废弃的秸杆等生产沼气 | |
| D. | 为防止电池中的重金属污染土壤,将废旧电池深埋地下 |
9.下列说法不正确的是( )
| A. | 增大压强,活化分子百分数不变,化学反应速率增大 | |
| B. | 升高温度,活化分子百分数增大,化学反应速率增大 | |
| C. | 增大反应物浓度,活化分子百分数增大,化学反应速率增大 | |
| D. | 使用催化剂,活化分子百分数增大,化学反应速率增大 |
6.化学与生活密切相关 下列应用中与盐类水解无关的是( )
| A. | 明矾净化水 | B. | 纯碱去油污 | C. | 食醋除水垢 | D. | 漂白粉漂白织物 |
7.下列实验中,对应的现象及结论都正确的是( )
| 实验 | 现 象 | 结 论 | |
| A | 向FeI2溶液中滴加KSCN溶液,再滴入1ml苯和少量氯水,振荡 | 苯层呈紫红色,下层为无色 | Fe2+ 的还原性强于I- |
| B | 向饱和碳酸钠溶液中通入CO2至饱和 | 溶液中有白色沉淀 | 白色沉淀为NaHCO3 |
| C | 向酸性碘酸钾溶液中加入淀粉,再缓慢通入过量SO2 | 溶液先变蓝,后蓝色又褪去 | 氧化性:IO-3>I2>SO2 |
| D | 足量的铝条加入热的浓硫酸中,然后冷却至室温 | 无气体产生 | 铝在浓硫酸中钝化 |
| A. | A | B. | B | C. | C | D. | D |
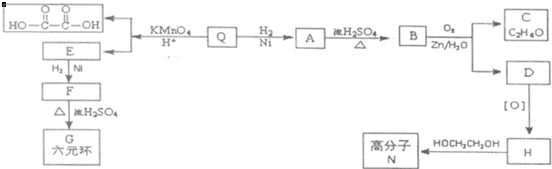
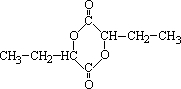 ;Q的反式结构简式是
;Q的反式结构简式是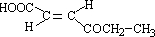 .
.
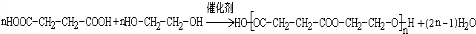 .
.