题目内容
0.200 mol某短周期元素M的单质与足量的盐酸反应,在标准状况下生成6.72 L氢气。等量的M元素的单质与足量的氧气化合,可生成10.2 g M元素的最高价氧化物,M元素中子数比质子数多一个。求M的核电荷数及在元素周期表中的位置。
M的核电荷数为13,它在周期表中的位置为第三周期第ⅢA族
由题意的氢气n =6.72L∕22.4L /mol=0.3mol
/mol=0.3mol
2M+2nHCl=2MCln+nH2↑
2 n
0.2 0.3
n=3……………(2分)
则氧化物的化学是为M2O3
 设生成氧化物的物质的量为x
设生成氧化物的物质的量为x
4M+3O2= 2M2O3
4mol 2mol
0.2mol x
x="0.05mol" ……………(2分)
所以 M2O3的相对分子质量为10.2/0.05=104
设M的相对原子质量为a,
则a×2+16×3="104 " a=27
又因为中子数比质子数多一个
设质子数为Z,则Z+Z+1="27 " Z=13
所以M在周期表中的位置为:第三周期第ⅢA族……………(3分)
答:M的核电荷数为13,它在周期表中的位置为第三周期第ⅢA族(1分)
 /mol=0.3mol
/mol=0.3mol2M+2nHCl=2MCln+nH2↑
2 n
0.2 0.3
n=3……………(2分)
则氧化物的化学是为M2O3
 设生成氧化物的物质的量为x
设生成氧化物的物质的量为x 4M+3O2= 2M2O3
4mol 2mol
0.2mol x
x="0.05mol" ……………(2分)
所以 M2O3的相对分子质量为10.2/0.05=104
设M的相对原子质量为a,
则a×2+16×3="104 " a=27

又因为中子数比质子数多一个
设质子数为Z,则Z+Z+1="27 " Z=13
所以M在周期表中的位置为:第三周期第ⅢA族……………(3分)
答:M的核电荷数为13,它在周期表中的位置为第三周期第ⅢA族(1分)

练习册系列答案
相关题目

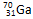 和
和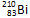 两原子经核聚合,并放出一定数目的中子而制得质量数为275,质子数为114的某原子。则两原子在核聚合过程中放出的中子数目是
两原子经核聚合,并放出一定数目的中子而制得质量数为275,质子数为114的某原子。则两原子在核聚合过程中放出的中子数目是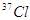 含有_____个质子,_____个中子,_____个电子。它的质量数等于_____。氯的最高价氧化物化学式为__________,气态氢化物的化学式为__________。
含有_____个质子,_____个中子,_____个电子。它的质量数等于_____。氯的最高价氧化物化学式为__________,气态氢化物的化学式为__________。
 (2)第一电离能最大的元素是________。
(2)第一电离能最大的元素是________。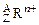 表示,下列
表示,下列 关于该微粒的叙述中正确的是
关于该微粒的叙述中正确的是
 。
。 。
。