题目内容
【题目】T1、T2两种温度下BaSO4在水中的沉淀溶解平衡曲线如图所示,请回答下列问题:
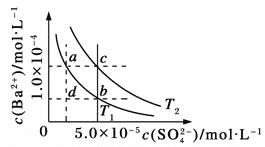
(1)T1________T2(填“>”、“<”或“=”),T2时Ksp(BaSO4)=____________。
(2)根据T1温度时BaSO4的沉淀溶解平衡曲线,判断下列说法正确的是________(填序号)。
A.加入Na2SO4可由a点变为b点
B.在T1曲线上方区域(不含曲线)的任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能由d点变为T1曲线上a、b之间的某一点(不含a、b)
D.升温可由b点变为d点
【答案】 T1<T2 5.0×10-9 ABC
【解析】溶度积常数只与温度有关系,结合曲线的变化趋势判断温度、计算溶度积,依据硫酸钡的溶度积常数表达式分析解答,据此分析判断。
(1)升高温度促进溶解,溶度积常数增大,则依据图像可知T1<T2,T2时根据c点对应的离子浓度可知Ksp(BaSO4)=c(SO42-)·c(Ba2+)=5×10-5×1×10-4=5.0×10-9;(2)A.加入Na2SO4硫酸根浓度增大,仍然是饱和溶液,则可由a点变为b点,A正确;B.在T1曲线上方区域(不含曲线)的任意一点时浓度积均大于溶度积,因此均有BaSO4沉淀生成,B正确;C.蒸发溶剂硫酸根、钡离子浓度均增大,因此可能由d点变为T1曲线上a、b之间的某一点(不含a、b),C正确;D.升温离子的浓度不变,不可能由b点变为d点,D错误,答案选ABC。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目