题目内容
5.设NA为阿伏加德罗常数,下列说法中,正确的是( )| A. | 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1NA | |
| B. | 标准状况下,1.12L氦气所含原子数为0.1NA | |
| C. | 17gNH3所含电子数目为NA | |
| D. | 22.4LHCl溶于水,溶液中H+数为NA |
分析 A、求出钠的物质的量,然后根据反应后钠元素变为+1价来分析;
B、氦气为单原子分子;
C、求出氨气的物质的量,然后根据1mol氨气中含10mol电子来分析;
D、HCl的状态不明确.
解答 解:A、23g钠的物质的量为1mol,而反应后钠元素变为+1价,故1mol钠转移1mol电子即NA个,故A正确;
B、氦气为单原子分子,故标况下1.12L氦气即0.05mol氦气中含0.05mol原子即0.05NA个,故B错误;
C、17g氨气的物质的量为1mol,而1mol氨气中含10mol电子即10NA个,故C错误;
D、HCl的状态不明确,故其物质的量不能计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
16.下列反应的离子方程式正确的是( )
| A. | 明矾净水:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 硫酸镁与氢氧化钡溶液混合:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| C. | 磷酸二氢钙与足量烧碱溶液反应:3Ca2++2H2PO${\;}_{4}^{-}$+4OH-═Ca3(PO4)2↓+4H2O | |
| D. | 氨水中通入过量的二氧化硫气体:NH3•H2O+SO2═NH${\;}_{4}^{+}$+HSO${\;}_{3}^{-}$ |
13.下列反应中,熵变小于0的是( )
| A. | (NH4 )2CO3(s)═NH4HCO3(s)+NH3(g) | B. | 2N2O5(g)═4NO2(g)+O2(g) | ||
| C. | MgCO3(s)═MgO(s)+CO2(g) | D. | 2CO(g)═2C(s)+O2(g) |
17.取a g某铁的氧化物R溶于足量的盐酸中,加水稀释至200mL,取20mL所得溶液,向其中滴加新制的氯水,将其中的铁元素全部氧化为Fe3+,再向溶液中加入NaOH溶液使其完全沉淀,所得沉淀经过过滤、洗涤,并将沉淀灼烧至质量不再改变,称量得b g固体,则下列判断正确的是( )
| A. | 若a:b=9:1,则R的化学式为FeO | |
| B. | 若a:b=1:10,则R的化学式为Fe2O3 | |
| C. | 若a:b=29:30,则R的化学式为Fe3O4 | |
| D. | 试验过程中被还原的Cl2为(10b-a)/8mol |
14.下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
| A. | 异戊二烯( )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 | |
| B. | 2-氯丁烷(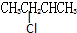 )与NaOH乙醇溶液共热发生消去HCl分子的反应 )与NaOH乙醇溶液共热发生消去HCl分子的反应 | |
| C. | 邻羟基苯甲酸与NaHCO3溶液反应 | |
| D. | 甲苯在一定条件下发生硝化生成一硝基甲苯的反应 |
 )是比较简单的稠环芳香烃.请回答以下问题:
)是比较简单的稠环芳香烃.请回答以下问题: