��Ŀ����
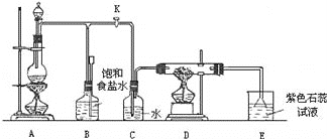
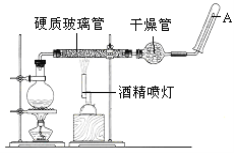
����Ŀ���ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe��ˮ�����ɷ�����Ӧ���������������������û���������Ӧ������װ�ã���Ӳ�ʲ������з��뻹ԭ���ۺ�ʯ���Ļ������ȣ���ͨ��ˮ�������Ϳ�����ɸ�������Fe��ˮ�����ķ�Ӧʵ������
��ش��ʵ���е����⡣
(1)д���÷�Ӧ�Ļ�ѧ����ʽ��________________________________________����������ԭ��Ӧ�Ļ�ԭ����_______________����������_______________ ��
(2)ʵ��ǰ���������װ�ý��еIJ�����_______________________��
(3)Բ����ƿ��ʢװ��ˮ����װ�����Ⱥ����Ҫ������____________________����ƿ�ײ������˼�Ƭ���Ƭ�����Ƭ��������_________________________________��
(4)�������ʢװ�ǵ�������________����д���ƣ���������__________��
���𰸡�3Fe+4H2O==Fe3O4+4H2 Fe H2O ���װ�õ������� �ṩˮ���� ��ֹ���� ��ʯ�� ��ȥˮ����
��������
��1������ˮ��������������ԭ��Ӧ�������������������������ݴ���д��ѧ����ʽ����ԭ�����ж��������ݻ��ϼ����ߵ����ʣ��������ǻ��ϼ۽��͵����ʣ�
��2���÷�Ӧ��Ϊˮ���������������������������ɣ�����ʵ��ǰ���������װ�ý��������Լ�飻
��3����Ӧ��Ϊˮ�������������ȵ�Ŀ��Ϊʵ���ṩˮ������
��4���������ʢװ�ǵ������Ǽ�ʯ�ң������dz�ȥˮ������
��1������ˮ��������������ԭ��Ӧ��3Fe+4H2O��g��![]() Fe 3O4+4H2�����ݻ��ϼ��������ж��������ͻ�ԭ���������Ļ��ϼ����ߣ�����������ԭ����ˮ����Ļ��ϼ۽��ͣ�ˮ�����������ʴ�Ϊ��3Fe+4H2O��g��
Fe 3O4+4H2�����ݻ��ϼ��������ж��������ͻ�ԭ���������Ļ��ϼ����ߣ�����������ԭ����ˮ����Ļ��ϼ۽��ͣ�ˮ�����������ʴ�Ϊ��3Fe+4H2O��g��![]() Fe 3O4+4H2��Fe��H2O��
Fe 3O4+4H2��Fe��H2O��
��2������ˮ������Ӧ�������������������������÷�Ӧ��Ϊˮ������������������������������ʵ��ǰ���������װ�ý��������Լ�飬�ʴ�Ϊ������װ�õ������ԣ�
��3����Ϊ��Ӧ��Ϊˮ��������������������ȵ�Ŀ�ľ���ΪӲ�ʲ�������Fe��ˮ�����ķ�Ӧʵ���ṩ�������ϵ�ˮ�������ʴ�Ϊ��Ϊʵ���ṩ�ṩ�������ϵ�ˮ������ ��ֹ�����¹ʵķ�����
��4���������ʢװ�ǵ������Ǽ�ʯ�ң������dz�ȥˮ�������ʴ�Ϊ����ʯ�ң���ȥˮ������

 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д�����Ŀ���������ƿ����������ೱ��Ӧ�������ȡ���֪���������ƣ�Ϊ��ɫ��ɫ�ᾧ��ĩ��������ˮ���������Ҵ������ѵ��л��ܼ��������¸���Ʒ���ȶ���������ϡ�����ɹ������⡣ijС��ͬѧ̽���������Ƶ��Ʒ������ʣ�
(1) �ס�����λͬѧ��ƵĹ�������ʵ�����Ʒ����£����в��ʽϵ͵���______(��A��B)
����A Ca (OH)2 (s) + H2O2 ![]() CaO2 (s) + 2H2O
CaO2 (s) + 2H2O
����B CaCl2 (s) + H2O2 ![]() CaO2 (s) + 2HCl
CaO2 (s) + 2HCl
����A���ò�Ʒ�д��Ȳ��ߣ�����������Ҫ�� ___________(�ѧʽ)
����������ȶ����������ַ���������5�����½���ʵ�飬ԭ�������______________��
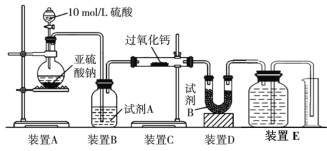
(2) ��ͬѧ��ΪCO2��SO2��������Ƶķ�Ӧԭ����ͬ����ͬѧ��ΪSO2���н�ǿ�Ļ�ԭ�ԣ���CO2û�У��ʶ���Ӧԭ������ͬ���������������ʵ��װ�ã�ͨ������װ��E��������������жϷ�Ӧ�����
���Լ�B��������____________________��
����ʵ����SO2����������������Ƴ�ַ�Ӧ��ȡ��Ӧ��Ĺ������̽��������֤����������SO2��Ӧ���������SO2δ����������Ӧ�Ļ�ѧ����ʽΪ��______________________________��
��װ��E���ռ������������ΪV L(�ѻ���ɱ�״����)����SO2��ȫ����������V =______��
(3)ij�������õ�ʯ��(��Ҫ�ɷ�Ϊ��������)�����������Ƶ������������£�

�������������Ʊ���������(CaO2��8H2O)�����貽���Ļ�ѧ����ʽ��______________��
�¶�(��) | 50 | 40 | 30 | 20 | 10 | 0 |
���� | 43.24 | 52.80 | 64.54 | 63.80 | 60.45 | 52.40 |
��ijС����õ�������ȷ���¶ȡ�H2O2Ũ�ȶԲ��ʵ�Ӱ�죬������£�
H2O2 % | 30% | 25% | 20% | 15% | 10% | 5% |
���� | 60.40 | 62.42 | 64.54 | 63.20 | 63.10 | 62.40 |
��ʵ������Ӧѡ���������Ϊ__________��