题目内容
“酒是陈的香”就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室和工业上常采用如下反应:CH3COOH+C2H5OH?CH3COOC2H5+H2O来制取乙酸乙酯.
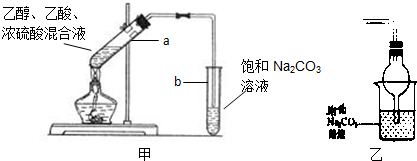
(1)实验时,试管B观察到的现象是界面处产生浅红色,下层为蓝色,振荡后产生气泡,界面处浅红色消失,原因是(用化学方程式表示)______.欲从上述混合物中分离出乙酸乙酯,采用的分离方法是______(填操作名称).
(2)事实证明,此反应以浓H2SO4为催化剂,也存在缺陷,其原因可能是______.
a.浓H2SO4易挥发,以至不能重复使用b.会使部分原料炭化
c.浓H2SO4有吸水性 d.会造成环境污染.
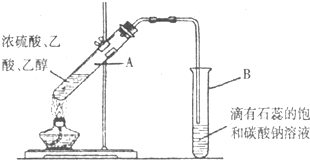
(1)实验时,试管B观察到的现象是界面处产生浅红色,下层为蓝色,振荡后产生气泡,界面处浅红色消失,原因是(用化学方程式表示)______.欲从上述混合物中分离出乙酸乙酯,采用的分离方法是______(填操作名称).
(2)事实证明,此反应以浓H2SO4为催化剂,也存在缺陷,其原因可能是______.
a.浓H2SO4易挥发,以至不能重复使用b.会使部分原料炭化
c.浓H2SO4有吸水性 d.会造成环境污染.

(1)试管B观察到的现象是界面处产生浅红色,说明是醋酸遇石蕊试液变红色,下层为蓝色是因为碳酸钠溶液呈碱性,振荡后产生气泡,界面处浅红色消失,醋酸和碳酸钠反应生成二氧化碳气体;乙酸乙酯难溶于水利用分液得到乙酸乙酯,故答案为:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O;分液;
(2)以浓H2SO4为催化剂,存在缺陷;
a、浓硫酸是难挥发性酸,故a不符合;
b、会使部分原料乙酸、乙醇炭化,故b符合;
c、浓硫酸的吸水性是有利于酯化反应.促进平衡正向进行,故c不符合;
d、浓硫酸和碳等物质反应生成二氧化硫等污染气体,造成环境污染,故d符合;
故答案为:bd.
(2)以浓H2SO4为催化剂,存在缺陷;
a、浓硫酸是难挥发性酸,故a不符合;
b、会使部分原料乙酸、乙醇炭化,故b符合;
c、浓硫酸的吸水性是有利于酯化反应.促进平衡正向进行,故c不符合;
d、浓硫酸和碳等物质反应生成二氧化硫等污染气体,造成环境污染,故d符合;
故答案为:bd.

练习册系列答案
相关题目