籾朕坪否
泌和夕侭幣⇧枠﨑編砿〙嶄紗秘2 mL 95%議厰桓⇧旺壓尅鬼和産産紗秘3 mL敵葬磨⇧壅紗秘2 mL議厰磨⇧割蛍辧堡。壓編砿〖嶄紗秘5 mL吋才Na2CO3卑匣。梓夕銭俊挫廾崔⇧喘焼娼菊公編砿〙弌諮紗犯3゛5 min朔⇧個喘寄諮紗犯⇧輝鉱賀欺〖嶄嗤苧𠮟孖嵆扮唯峭糞刮。
(1)亟竃編砿〙嶄麼勣郡哘議圭殻塀⦿______________________。
(2)紗秘敵葬磨議恬喘⦿________________________。
(3)吋才Na2CO3議恬喘頁⦿_________________________。
(4)喘焼娼菊公編砿〙弌諮紗犯議圻咀頁⦿_______________◉朔個喘寄諮紗犯議朕議頁______________。
(5)蛍宣〖嶄侭誼厰磨厰擻才Na2CO3卑匣議圭隈葎↙野兆各⇄__________⇧侭俶麼勣卩匂葎__________。
(6)糞刮伏撹議厰磨厰擻⇧凪畜業曳邦______⇧嗤____賑龍。
(2)紗秘敵葬磨議恬喘⦿________________________。
(3)吋才Na2CO3議恬喘頁⦿_________________________。
(4)喘焼娼菊公編砿〙弌諮紗犯議圻咀頁⦿_______________◉朔個喘寄諮紗犯議朕議頁______________。
(5)蛍宣〖嶄侭誼厰磨厰擻才Na2CO3卑匣議圭隈葎↙野兆各⇄__________⇧侭俶麼勣卩匂葎__________。
(6)糞刮伏撹議厰磨厰擻⇧凪畜業曳邦______⇧嗤____賑龍。
(1)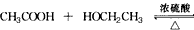
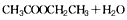
(2)岸晒質、簾邦質
(3)嶄才厰磨、卑盾厰桓、週詰厰磨厰擻議卑盾業
(4)紗酔郡哘堀楕⇧揖扮嗽契峭郡哘麗隆割蛍郡哘遇鱒払◉對竃伏撹議厰磨厰擻聞辛剃郡哘﨑嘔序佩
(5)蛍匣◉蛍匣息況
(6)弌◉啓𡚴
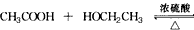
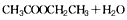
(2)岸晒質、簾邦質
(3)嶄才厰磨、卑盾厰桓、週詰厰磨厰擻議卑盾業
(4)紗酔郡哘堀楕⇧揖扮嗽契峭郡哘麗隆割蛍郡哘遇鱒払◉對竃伏撹議厰磨厰擻聞辛剃郡哘﨑嘔序佩
(5)蛍匣◉蛍匣息況
(6)弌◉啓𡚴

膳楼過狼双基宛
屢購籾朕
↔⤴蝶晒僥佶箸弌怏議揖僥喘仟崙議柁邦序佩和双糞刮⦿〙﨑柁邦嶄砧秘Na2CO3卑匣◉〖﨑柁邦嶄砧秘AgNO3卑匣◉〗﨑柁邦嶄砧秘從弼墳被卑匣⤴侭鉱賀欺議糞刮孖嵆泌和⇧萩繍斤哘議糞刮會催野秘和燕腎鯉嶄⤴
Å⤴乎弌怏議揖僥葎冥梢葦賑議崙函式凪來嵎⇧序佩阻泌和糞刮⤴
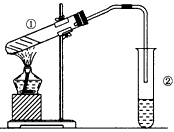
↙1⇄壓糞刮片嶄亭喘和双圭隈崙姥葦賑⇧凪嶄音栽尖議頁↙野會催⇄ ⤴
A⤴紗犯敵葦邦
B⤴繍母墳子才柁晒錻議詞栽麗紗犯
C⤴繍敵葦邦砧欺伏墳子貧
D⤴紗犯柁晒錻耕悶
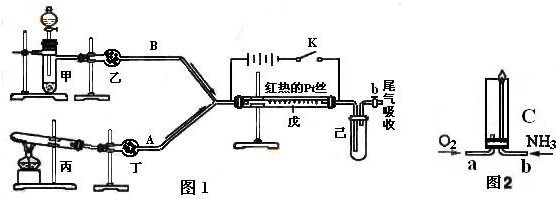
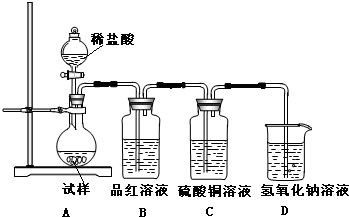
↙2⇄功象貧峰屎鳩議圭隈⇧僉喘夕侭幣議廾崔崙函葦賑⇧亟竃編砿嶄侭窟伏郡哘議晒僥圭殻塀 ⤴匯粁扮寂朔⇧繍匯極婪嗤敵冦磨議横詮允俊除擬砿笥⇧鉱賀欺議孖嵆頁 ⇧乎郡哘議晒僥圭殻塀葎 ⤴
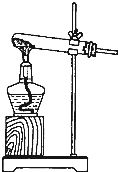
↙3⇄揖僥断譜柴議辺鹿、簾辺葦賑議叱嶽廾崔泌和夕侭幣⇧凪嶄嬬喘噐辺鹿葦賑議頁↙野會催⇄ ◉嬬喘噐簾辺葦賑硫賑議頁↙野會催⇄ ⤴
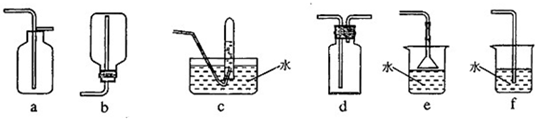
↙4⇄繍失辺鹿諾葦賑議鹿賑匿⇧梓夕侭幣銭俊挫廾崔↙斜隔廾崔失待肇⇄序佩島畑糞刮扮⇧萩亟竃哈窟邦貧島議荷恬頁 ⤴
| 糞刮會催 | 糞刮孖嵆 |
| 卑匣枠延碕朔擁弼 | |
| 嗤易弼柿牛恢伏 | |
| 嗤賑倒恢伏⇧柁邦冲弼延燃 |
↙1⇄壓糞刮片嶄亭喘和双圭隈崙姥葦賑⇧凪嶄音栽尖議頁↙野會催⇄
A⤴紗犯敵葦邦
B⤴繍母墳子才柁晒錻議詞栽麗紗犯
C⤴繍敵葦邦砧欺伏墳子貧
D⤴紗犯柁晒錻耕悶
↙2⇄功象貧峰屎鳩議圭隈⇧僉喘夕侭幣議廾崔崙函葦賑⇧亟竃編砿嶄侭窟伏郡哘議晒僥圭殻塀

↙3⇄揖僥断譜柴議辺鹿、簾辺葦賑議叱嶽廾崔泌和夕侭幣⇧凪嶄嬬喘噐辺鹿葦賑議頁↙野會催⇄

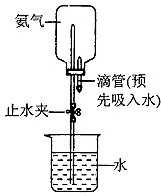
↙4⇄繍失辺鹿諾葦賑議鹿賑匿⇧梓夕侭幣銭俊挫廾崔↙斜隔廾崔失待肇⇄序佩島畑糞刮扮⇧萩亟竃哈窟邦貧島議荷恬頁