题目内容
实验室里常见到如下图所示的仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。
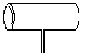 用该仪器可进行多项实验,当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,它具有装置简单、操作方便、现象明显、没有污染、可反复使用等优点。试完成下列空白:
用该仪器可进行多项实验,当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,它具有装置简单、操作方便、现象明显、没有污染、可反复使用等优点。试完成下列空白:
(1)用此仪器不能反复进行的实验是 ( )。
A.NH4Cl固体受热分解
B.KMnO4晶体受热分解
C.白磷和红磷在一定温度下互相转化
D.无水CuSO4和胆矾的互变实验
(2)当玻璃管内装有NO2和N2O4的混合气体时,可反复进行反应条件对化学平衡影响的实验。该实验的操作过程和实验现象是________________________。
(3)如果玻璃管内装有少量某红色溶液,加热时溶液的颜色逐渐变浅,冷却后恢复红色,该溶液可能是________________;如果玻璃管内装有少量某无色溶液,加热溶液时,溶液变为红色,冷却后恢复无色,则此溶液可能是________________。
(1)B
(2)当玻璃管内装有NO2和N2O4的混合气体时,把玻璃管放入冷水中,玻璃管内气体颜色变浅;把玻璃管放入热水中,玻璃管内气体颜色变深
(3)稀氨水和酚酞试液;溶有SO2的品红试液
【试题分析】
解析:理解反应原理、把握仪器特点是解决问题的根本。
(1)用此仪器做碘升华实验时,物质的变化过程:仪器受热,晶体碘变为碘蒸气;仪器冷却后,碘蒸气又转化为固体。这样,可概括出能用此仪器做的实验必须满足下列条件:受热时发生变化,产生新物质或改变状态;新物质或新状态在冷却过程中(或温度有变化的条件下)又可恢复为原来的物质或状态。故答案为B。
(2)根据勒夏特列原理,影响化学平衡的条件通常有“温度、压强、浓度”,因为该仪器是一固定容积的密闭容器,故采用改变压强或浓度的方法是行不通的,只有选择改变温度这一途径。
(3)本题涉及物质的溶解平衡问题。首先要审清实验的装置为一密闭容器,受热时,有气体从溶液中逸出,导致溶液的颜色变化;冷却后,逸出的气体又溶解于溶液中,得到原溶液,恢复为原来溶液的颜色。另外,还要注意溶液颜色的变化情况。

练习册系列答案
相关题目
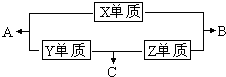 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:

